题目内容
【题目】氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下图所示。

回答下列问题:
(1)CuCl中Cu元素在周期表中的位置为___________。
(2)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为________。溶解温度应控制在60~70℃,原因是______________。
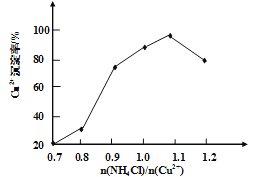
(3)写出步骤③中主要反应的离子方程式________。(NH4)2SO3要适当过量,目的有:保证Cu2+的还原速率,__________。已知NH4Cl、Cu2+的物质的量之比![]() 与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是________。
与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是________。
(4)步骤⑥加入乙醇洗涤的目的是__________。
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解;
②用0.100mol·L-1硫酸铈[Ce(SO4)2]标准溶液测定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
平衡实验次数 | 1 | 2 | 3 |
0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为_______(结果保留3位有效数字)。
【答案】 第四周期第IB族 4Cu+NO3-+10H+=4Cu2-+NH4-+3H2O 温度低溶解速度慢、温度过高铵盐分解 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+ 防止CuCl被空气氧化 生成的氯化亚铜又溶解于氯化铵溶液中 醇洗有利于加快除去CuCl表面的水分,防止其水解氧化 95.5%
【解析】酸性条件下硝酸根离子具有氧化性,可氧化海绵铜(主要成分是Cu和少量CuO)生成硫酸铜,过滤后在滤液中加入亚硫酸铵发生氧化还原反应生成CuCl,发生2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+,得到的CuCl经硫酸酸洗,水洗后再用乙醇洗涤,烘干得到氯化亚铜。
(1)CuCl中Cu元素在周期表中的位置为第四周期第IB族,故答案为:第四周期第IB族;
(2)步骤①中由于酸性条件下硝酸根离子具有氧化性,可氧化Cu生成CuSO4,反应为4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O,离子方程式为4Cu+NO3-+10H+=4Cu2-+NH4-+3H2O。温度低溶解速度慢、温度过高铵盐分解,因此溶解温度应控制在60~70℃,故答案为:4Cu+NO3-+10H+=4Cu2-+NH4-+3H2O;温度低溶解速度慢、温度过高铵盐分解;
(3)步骤③中铜离子与亚硫酸铵发生氧化还原反应生成CuCl,发生2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+,(NH4)2SO3要适当过量,目的有:保证Cu2+的还原速率,防止CuCl被空气氧化;当氯化铵用量增加到一定程度后氯化亚铜的沉淀率减少,原因是生成的氯化亚铜又溶解于氯化铵溶液中,故答案为:2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+;防止CuCl被空气氧化;生成的氯化亚铜又溶解于氯化铵溶液中;
(4)步骤⑥加入乙醇洗涤,因乙醇沸点低,易挥发,则用乙醇洗涤,可快速除去固体表面的水分,防止水解、氧化,故答案为:醇洗有利于加快除去CuCl表面的水分,防止其水解氧化;
(5)根据题目中所给数据及平行实验结果相差不能超过1%,体积为24.35mL,误差大舍去,滴定0.25g样品消耗硫酸铈标准溶液的平均体积为24.00mL,结合方程式可知:CuCl+FeCl3═CuCl2+FeCl2,CuCl的纯度为24×10-3L×0.1 molL-1×99.5gmol-1÷0.25g×100%=95.5%;故答案为:95.5%。

 阅读快车系列答案
阅读快车系列答案【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
序号 | ||||
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是_________(填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。

①门捷列夫将已有元素按照相对原子质量排序,同一_________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_________,第5列方框中“Te=128?” 的问号表达的含义是_________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_________(填字母序号)。
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5。其余信息如图所示:

①上述七种元素中,处于第二周期的有_________(用元素符号表示,下同),X在周期表中的位置是_________。
②E的原子结构示意图为_________,写出Z元素气态氢化物的电子式:_________。
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为_________;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为_________。
④B和D的最高价氧化物的水化物的化学式分别为_________、_________,二者酸性前者_________(填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: _________。
【题目】已知实验室制备1,2﹣二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.现在用溴的CCl4溶液和足量的乙醇制备1,2﹣二溴乙烷的装置如下图所示:
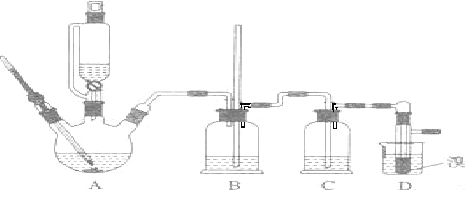
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:
(1)制备1,2﹣二溴乙烷的合成路线
(2)在装置C中应加入 ,(填正确选项前的字母)其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)装置B的作用是 ;
(4)若产物中有少量副产物乙醚.可用 的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 .