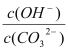��Ŀ����
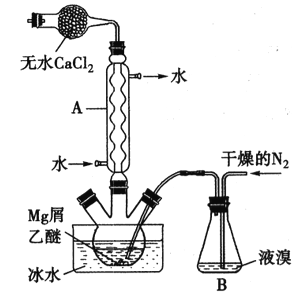
����Ŀ����֪ʵ�����Ʊ�1��2������������ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������l40����ˮ�������ѣ����������CCl4��Һ���������Ҵ��Ʊ�1��2�����������װ������ͼ��ʾ��

�й������б����£�
�Ҵ� | 1��2���������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/gcm��3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | һl30 | 9 | ��1l6 |
�ش��������⣺
(1)�Ʊ�1��2����������ĺϳ�·��
(2)��װ��C��Ӧ���� ��(����ȷѡ��ǰ����ĸ)��Ŀ����
a��ˮ b��Ũ���� c������������Һ d������̼��������Һ
(3)װ��B�������� ��
(4)�����������������������ѣ����� �ķ�����ȥ��
(5)��Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ���� �����ֲ��ܹ�����ȴ(���ñ�ˮ)����ԭ���� ��
���𰸡�(1)CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br
BrCH2CH2Br
(2) c ���շ�Ӧ�п������ɵ��������� (3)��ֹ����(4) ����
(5) ��ȴ�ɱ�����Ĵ����ӷ� 1��2������������۵�ͣ�������ȴ�����̶���������
��������
���������(1)ʵ�����Ʊ�1��2-��������ķ�Ӧԭ��Ϊ���ȷ����Ҵ�����ȥ��Ӧ������ϩ���ٷ�����ϩ����ˮ�ļӳɷ�Ӧ���ϳ�·��ΪCH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br[��
BrCH2CH2Br[��
(2)Ũ�������ǿ�����ԣ����Ҵ������ɶ�����̼����������ԭ�ɶ�����������̼�����������ܺ�����������Һ��Ӧ�������գ���װ��C���Լ�ΪNaOH��Һ����Ŀ�������շ�Ӧ�п������ɵ�����������
(3)װ��B�г����ܵ������Ƿ�������
(4)���߾�Ϊ�л�����ܣ���1��2-�������������ѵķе㲻ͬ��������ķ��������Ƿ��룻
(5)���ڳ����£��ӷ�����ϩ���巴Ӧʱ���ȣ�����ӷ�����ȴ�ɱ�����Ĵ����ӷ�����1��2-������������̵�9���ϵͣ����ܹ�����ȴ��������ȴ��ʹ�����̶�ʹ��·����������B�г�������Һ��������

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
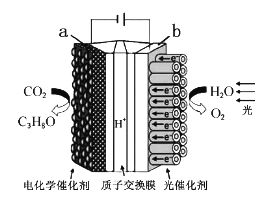
Сѧ��10����Ӧ����ϵ�д�����Ŀ���Ȼ���ͭ��CuCl���㷺���ڻ�����ӡȾ���л��ϳɵ���ҵ��CuCl�����ڴ���ˮ��������������Ũ�Ƚϴ����ϵ���ڳ�ʪ��������ˮ���������Ժ���ͭ����Ҫ�ɷ���Cu������CuO��Ϊԭ�ϣ���������������ֽ⼼�������Ȼ���ͭ�Ĺ��չ�������ͼ��ʾ��
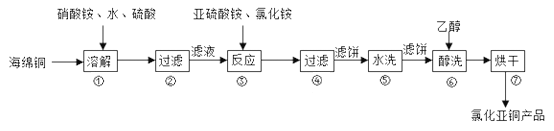
�ش��������⣺
��1��CuCl��CuԪ�������ڱ��е�λ��Ϊ___________��
��2���������NԪ�ر���ԭΪ��ͼۣ���Cu�ܽ�����ӷ���ʽΪ________���ܽ��¶�Ӧ������60~70�棬ԭ����______________��
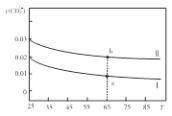
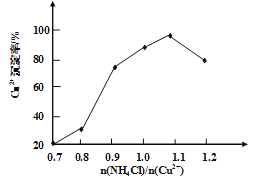
��3��д�����������Ҫ��Ӧ�����ӷ���ʽ________��(NH4)2SO3Ҫ�ʵ�������Ŀ���У���֤Cu2+�Ļ�ԭ���ʣ�__________����֪NH4Cl��Cu2+�����ʵ���֮��![]() ��Cu2+�����ʵĹ�ϵ��ͼ��ʾ�����Ȼ���������ӵ�һ��Ũ�Ⱥ��Ȼ���ͭ�ij����ʼ��٣�ԭ����________��
��Cu2+�����ʵĹ�ϵ��ͼ��ʾ�����Ȼ���������ӵ�һ��Ũ�Ⱥ��Ȼ���ͭ�ij����ʼ��٣�ԭ����________��
��4����������Ҵ�ϴ�ӵ�Ŀ����__________��
��5���Ȼ���ͭ�Ķ���������
�ٳ�ȡ��Ʒ0.250g��10mL������FeCl3��Һ��250mL��ƿ�У�����ܽ⣻
����0.100mol��L��1������[Ce(SO4)2]����Һ�ⶨ����֪��CuCl+FeCl3=CuCl2+FeCl2��Fe2++Ce4+=Fe3++Ce3+��
����ƽ��ʵ�������±���ƽ��ʵ�������ܳ���1%����
ƽ��ʵ����� | 1 | 2 | 3 |
0.250g��Ʒ�������������Һ�������mL�� | 24.35 | 24.05 | 23.95 |
����Ʒ��CuCl�Ĵ���Ϊ_______���������3λ��Ч���֣���