题目内容
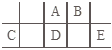
【题目】短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法正确的是( )
A.A的氢化物沸点比D的高,因为A的氢化物分子内存在氢键
B.工业上常用C与E形成的化合物来获得C的单质
C.简单离子的半径由大到小为:E>A>B>C
D.D、E两元素形成的化合物每种原子最外层一定都达到了8e-稳定结构
【答案】C
【解析】
设D原子M层电子数是x,D原子的质子数是10+x,D原子的质子数是其M层电子数的三倍,则10+x=3x,x=5,所以D是P元素;根据短周期元素A、B、C、D、E在元素周期表中的相对位置,可知A、B、C、D、E分别是N、O、Al、P、Cl。
A. NH3的沸点比PH3高,因为NH3分子间存在氢键,故A错误;
B. 工业上常用电解熔融Al2O3来获得Al单质,故B错误;
C. 简单离子的半径由大到小为:Cl->N3->O2->Al3+,故C正确;
D. P、Cl两元素形成的化合物PCl5,P原子最外层没有达到了8e-稳定结构,故D错误。

 阅读快车系列答案
阅读快车系列答案【题目】已知1g氢气完全燃烧生成液态水时放出热量143kJ,18g水蒸气变成液态水放出44kJ的热量。其他相关数据如下表:
化学键 | O=O | H—H | H—O(g) |
1 mol化学键断裂时 需要吸收的能量/kJ | 496 | x | 463 |
则表中x为( )
A.920B.557C.436D.188
【题目】在一定条件下发生反应:4NO2(g)+O2(g)![]() 2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
时间/s | 0 | 5 | 10 | 15 |
c(NO2)/(mol·L-1) | 4.00 | 2.52 | 2.00 | c3 |
c(O2)/(mol·L-1) | 1.00 | c1 | c2 | 0.50 |
(1)0~10s内N2O5的平均反应速率为__ ,此温度下的平衡常数为___。
(2)其他条件不变,将容器体积压缩一半,则重新达到平衡时c(N2O5)___2.00mol·L-1(填“>、<或=”,下同)
(3)假设温度T1时平衡常数为K1,温度T2时平衡常数为K2,若K1<K2,则T1____T2。
(4)下列可以作为平衡的依据的是___
A.容器内混合气体的颜色不再改变
B.生成1molO2的同时消耗2molN2O5
C.混合气体的平均摩尔质量不再变化
D.混合气体的密度不再变化
(5)改变哪些措施可以增加NO2的平衡转化率___(答出任意两条及以上)
(6)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol1
2C(s)+O2(g)=2CO(g) ΔH=﹣221.0 kJ·mol1
C(s)+O2(g)=CO2(g) ΔH=﹣393.5 kJ·mol1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=___ kJ·mol1,利于该反应自发进行的条件是___(选填“高温”或“低温”)。