题目内容
w g铁粉和铝粉的混合物,和过量的 NaOH反应,然后过滤,将沉淀完全收集后,放蒸发皿中加热,直至被加热的物质质量不再变化,取出蒸发皿中的物质称量仍为w g。求原混合物中铝粉的质量分数是( )
| A.30% | B.50% | C.70% | D.90% |
A
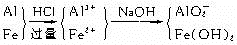 由于合金的质量等于Fe2O3的质量,且Fe完全转化至Fe2O3中,故原合金中Al元素的质量必然等于Fe2O3中O元素的质量,则合金中Al的含量为:
由于合金的质量等于Fe2O3的质量,且Fe完全转化至Fe2O3中,故原合金中Al元素的质量必然等于Fe2O3中O元素的质量,则合金中Al的含量为:

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
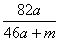 %
%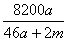 %
%