题目内容
7.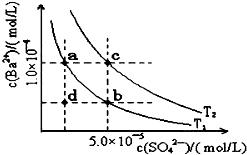 已知BaSO4(s)?Ba2+(aq)+SO4 2-(aq),25℃时Ksp=1.07×10-10,且BaSO4的随温度升高而增大.如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线,则下列说法不正确的是( )
已知BaSO4(s)?Ba2+(aq)+SO4 2-(aq),25℃时Ksp=1.07×10-10,且BaSO4的随温度升高而增大.如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线,则下列说法不正确的是( )| A. | 温度为T1时,在T1曲线上方区域任意一点时,均有BaSO4沉淀生成 | |
| B. | 蒸发溶剂可能使溶液由d点变为T1曲线上a、b之间的某一点 | |
| C. | 升温可使溶液由b点变为d点 | |
| D. | T2>25℃ |
分析 A.在T1曲线上方区域(不含曲线)为过饱和溶液;
B.蒸发溶剂,增大溶液中溶质的浓度,温度不变,溶度积常数不变;
C.升温增大溶质的溶解,溶液中钡离子、硫酸根离子浓度都增大;
D.根据图片知,温度越高,硫酸钡的溶度积常数越大,根据T2时硫酸钡溶度积常数与 25C时溶度积常数比较判断.
解答 解:A.在T1曲线上方区域(不含曲线)为过饱和溶液,所以有晶体析出,故A正确;
B.蒸发溶剂,增大溶液中溶质的浓度,温度不变,溶度积常数不变,所以蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b),故B正确;
C.升温增大溶质的溶解度,溶液中钡离子、硫酸根离子浓度都增大,故C错误;
D.25°C时硫酸钡的Ksp=1.07×10-10,根据图片知,温度越高,硫酸钡的离子积常数越大,T2时硫酸钡的溶度积常数=1.0×10-4×5.0×10-5=5×10-9>1.07×10-10,所以该温度大于25℃,故D正确;
故选C.
点评 本题考查了难溶电解质的溶解平衡及其应用,题目难度中等,正确理解溶度积曲线是解本题关键,结合溶度积常数来分析解答,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
18.酸和醇可以发生酯化反应,生成酯类物质,下列酸和醇能生成相对分子质量为90的酯的是( )
| A. | CH3C18OOH与C2H518OH | B. | CH3C18O18OH与C2H518OH | ||
| C. | CH3CO18OH与C2H518OH | D. | CH3CO18OH 与C2H5OH |
15.下列说法错误的是( )
| A. | 乙烷和丙烯的物质的量共1mol,完全燃烧可生成3molH2O | |
| B. | 等质量的乙烯与聚乙烯完全燃烧,产生的CO2质量相等 | |
| C. | 乙醇和乙醚互为同分异构体 | |
| D. | 用水可区分苯和四氯化碳 |
2.下列化学用语描述中不正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}Cl$ | |
| B. | K2O的电子式: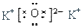 | |
| C. | HCO3-的电离方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 比例模型 可以表示CO2分子或SiO2 可以表示CO2分子或SiO2 |
16.蒸干并灼烧下列物质的水溶液,仍能得到该物质的是( )
| A. | 氯化铝 | B. | 碳酸氢钠 | C. | 硫酸亚铁 | D. | 碳酸钠 |
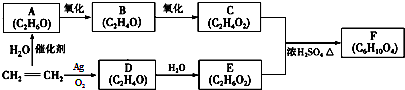
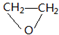 .
.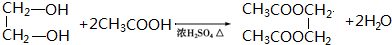 .
.