题目内容
【题目】金、银、铜、铁、铝和钛均是人类大量生产和使用的金属。试回答与上述金属原子结构有关的问题:
(1)上述金属中属于主族元素的有________。
(2)钛被称为继铁、铝之后的第三金属。基态钛原子外围电子的电子排布图为_____________。
(3)基态金原子的外围电子排布式为5d106s1,试判断金在元素周期表中位于第_____周期第____族。
(4)已知Ag与Cu位于同一族,则Ag在元素周期表中位于________区(填“s”、“p”、“d”、“f”或“ds”)。
【答案】 铝 ![]() 六 ⅠB ds
六 ⅠB ds
【解析】
(1)铝位于第三周期第ⅢA族,属于主族元素,金、银、铜、铁、和钛都不属于主族元素,
因此,本题正确答案是:铝。
(2)钛基态原子核外电子排布式为![]() ,其外围电子排布式为
,其外围电子排布式为![]() ,则其外围电子的电子排布图为:
,则其外围电子的电子排布图为:![]() ,
,
因此,本题正确答案是:![]() 。
。
(3)电子排布式中最大能层数与周期数相等,外围电子排布式为![]() 的原子位于第IB族,基态金原子的外围电子排布式为
的原子位于第IB族,基态金原子的外围电子排布式为![]() ,该原子最大能层数是6,所以金原子位于第6周期第ⅠB族,因此,本题正确答案是:6;ⅠB。
,该原子最大能层数是6,所以金原子位于第6周期第ⅠB族,因此,本题正确答案是:6;ⅠB。
(4)ⅠA、ⅡA族最后填充s电子,为s区;ⅢA~零族为p区,第ⅢB~ⅤⅡB族和第ⅤⅢ为d区;ⅠB和ⅡB族为ds区,Ag与Cu位于同一族,属于第ⅠB族,所以属于ds区,因此,本题正确答案是:ds。
点睛:(1)铝属于主族元素;(2)钛基态原子核外电子排布式为![]() ,其外围电子排布式为
,其外围电子排布式为![]() ;(3)电子排布式中能层数与周期数相等,外围电子排布式为
;(3)电子排布式中能层数与周期数相等,外围电子排布式为![]() 的原子位于第IB族;(4)ⅠA、ⅡA族最后填充s电子,为s区;ⅢA~零族为p区,第ⅢB~ⅤⅡB族和第ⅤⅢ为d区;ⅠB和ⅡB族为ds区。
的原子位于第IB族;(4)ⅠA、ⅡA族最后填充s电子,为s区;ⅢA~零族为p区,第ⅢB~ⅤⅡB族和第ⅤⅢ为d区;ⅠB和ⅡB族为ds区。

 快捷英语周周练系列答案
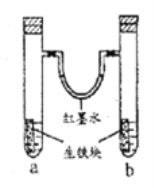
快捷英语周周练系列答案【题目】黄铁矿石的主要成分为FeS2和少量FeS(假设其它杂质中不含铁、硫元素,且高温下不发生化学变化),它是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2,4FeS+7O2=2Fe2O3+4SO2
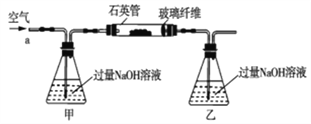
(实验一)测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:
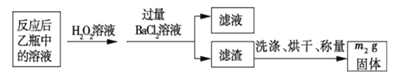
(1)鼓入空气的作用是_____________________。
(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是___________(用化学方程式表示)。H2O2可以看成是一种很弱的酸,写出其主要的电离方程式为____________________。
(3)该黄铁砂石中硫元素的质量分数为____________________(列出表达式即可)。
(实验二)测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤 ③将过滤液稀释至250mL
④取25.00mL稀释液,用0.100mol·L-1的酸性KMnO4溶液滴定
(4)步骤②中,若用铁粉作还原剂,则所测得的铁元素的含量__________(填“偏大”“ 偏小” 或“无影响”)。
(5)请写出步骤②中洗涤的方法____________________。
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
第一次 | 第二次 | 第三次 | 第四次 | |
消耗KMnO4溶液体积/ml | 25.00 | 25.03 | 20.00 | 24.97 |
根据所给数据,计算该稀释液中Fe2+的物质的量浓度c(Fe2+)=__________。