题目内容
【题目】氨是一种重要的化工产品。
(1)标准状况下,1 mol NH3的体积约为________L。
(2)实验室制取NH3的化学方程式为______________。
(3)收集NH3应使用________法,要得到干燥的NH3可选用___做干燥剂。
(4)压强对合成氨反应具有重要的影响。下表是反应达到平衡时压强与 NH3 含量的一些实验数据:
压强MPa | 10 | 20 | 30 | 60 | 100 |
NH3含量(体积分数%) | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
从表中数据可以推断:随着压强增大,平衡时NH3含量随之___(填字母)。
A.增大 B.减小 C.先增大再减小 D.不变
【答案】22.4 2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O 向下排空气 碱石灰 A
2NH3↑+CaCl2+2H2O 向下排空气 碱石灰 A
【解析】
(1)标准状况下,1 mol NH3的体积约为![]() ,故答案为:22.4L;
,故答案为:22.4L;
(2)实验室制取NH3通常是用Ca(OH)2和NH4Cl共热来制备,其化学方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O,故答案为:2NH4Cl+Ca(OH)2
2NH3↑+CaCl2+2H2O,故答案为:2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;
2NH3↑+CaCl2+2H2O;
(3)由于氨气极易溶于水,密度比空气的小,故收集NH3应使用向下排空气法;由于氨气是碱性气体,能与酸性干燥剂反应,故要得到干燥的NH3可选用碱性干燥剂如碱石灰(CaO或固体NaOH等)来干燥,故答案为:向下排空气;碱石灰;
(4)从表中数据可以看出:随着压强增大,平衡时NH3含量随之增大,故答案为:A。

【题目】天然气水蒸汽重整法是工业上生产氢气的重要方法,反应在 400℃以上进行。l 00kPa 时,在反应容器中通入甲烷与为水蒸汽体积比为1 : 5的混合气体,发生下表反应。
反应方程式 | 焓变△H(kJ/mol) | 600℃时的平衡常数 |
①CH4(g)+ H2O(g) | a | 0.6 |
②CH4(g)+ 2H2O(g) | +165.0 | b |
③CO(g)+ H2O(g) | -41.2 | 2.2 |
请回答下列下列问题:
(1)上表中数据 a=__________; b= ___________ 。
(2)对于反应②,既能加快反应又能提高CH4转化率的措施是_____________。
A.升温 B.加催化剂 C.加压 D.吸收CO2
(3)下列情况能说明容器中各反应均达到平衡的是___________。
A.体系中H2O与CH4物质的量之比不再变化
B.体系中H2的体积分数保持不变
C.生成n 个CO2的同时消耗2n个H2O
D. v正(CO)= v逆(H2)
(4)工业重整制氢中,因副反应产生碳会影响催化效率,需要避免温度过高以减少积碳。该体系中产生碳的反应方程式为 _______________。
(5)平衡时升温,CO含量将_________(选填“增大”或“减小”)。
(6)一定温度下 ,平衡时测得体系中 CO2和H2的物质的量浓度分别是0.75mo l/L、4.80mol/L , 则此时体系中CO 物质的量浓度是_______ mol/L。
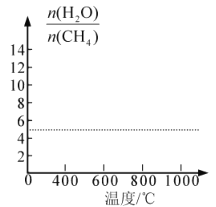
(7)改变上述平衡体系的温度,平衡时H2O与CH4物质的量之比[![]() ]值也会随着改变,在图中画出其变化趋势。________________
]值也会随着改变,在图中画出其变化趋势。________________