题目内容
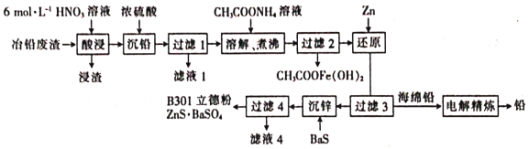
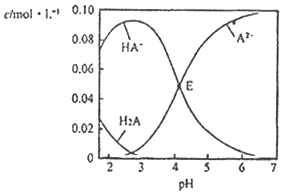
【题目】某酸H2A为二元弱酸.20℃时,配制一组c(H2A)+c(HA﹣)+c(A2﹣)=0.100molL﹣1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
A.pH=2.5的溶液中:c(H2A)+c(A2﹣)>c(HA﹣)
B.c(Na+)=0.100moLL﹣1的溶液中:c(H+)+c(H2A)=c(OH﹣)+c(A2﹣)
C.c(HA﹣)=c(A2﹣)的溶液中:c(Na+)>0.100molL﹣1+c(HA﹣)
D.pH=7.0的溶液中:c(Na+)<2c(A2﹣)
【答案】B
【解析】
A.根据图像知pH=2.5的溶液中:c(H2A)+ c(A2-)< c(HA -),A错误;
B. c(Na+)=0.100 mol·L-1的溶液,根据c(H2A)+ c(HA -)+ c(A2-)=0.100 mol·L-1知此时溶液中的溶质为NaHA,溶液中存在质子守恒:c(H+)+c(H2A)=c(OH-)+ c A2-),B正确;
C. c(HA-)= c(A2-)的溶液中有电荷守恒:c(OH-)+ c(HA-)+ 2c(A2-)=c(Na+)+c(H+),已知c(H2A)+ c(HA-)+ c(A2-)=0.100 mol·L-1,此溶液中H2A浓度几乎为0,可以忽略,把c(HA-)= c(A2-)和c(HA-)+ c(A2-)=0.100 mol·L-1带入电荷守恒的等式,得到:c(OH-)+ c(HA-)+ 0.100 mol·L-1=c(Na+)+c(H+),溶液的pH<7,c(H+) >c(OH-),所以c(Na+)<0.100 mol·L-1+ c(HA-),C错误;
D.pH=7时,c(H+)=c(OH-),根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)可知:c(Na+)=c(HA-)+2c(A2-),则c(Na+)>2c(A2-),D错误。
答案选B。

【题目】氨是一种重要的化工产品。
(1)标准状况下,1 mol NH3的体积约为________L。
(2)实验室制取NH3的化学方程式为______________。
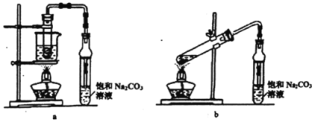
(3)收集NH3应使用________法,要得到干燥的NH3可选用___做干燥剂。
(4)压强对合成氨反应具有重要的影响。下表是反应达到平衡时压强与 NH3 含量的一些实验数据:
压强MPa | 10 | 20 | 30 | 60 | 100 |
NH3含量(体积分数%) | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
从表中数据可以推断:随着压强增大,平衡时NH3含量随之___(填字母)。
A.增大 B.减小 C.先增大再减小 D.不变