题目内容
9.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与催化剂接触面积 有关.
分析 (1)二氧化锰是过氧化氢分解的催化剂,由带火星木条复燃,可知产物,由此可写出方程式;由实验现象可知,反应放热还是吸热;
(2)由实验现象可知催化剂作用大小的影响因素.
解答 解:(1)H2O2在二氧化锰作用下发生反应的化学反应方程式为:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑,根据触摸试管的感觉可知,该反应为放热反应;
故答案为:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑; 放热;
(2)因在其他条件相同时,粉末状二氧化锰比块状二氧化锰反应所需时间短,说明催化剂接触面积对反应速率有影响,
故答案为:催化剂接触面积.
点评 本题考查通过化学实验分析催化剂影响化学反应速率的问题,题目难度中等,注意把握由数据及反应现象推断结论.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
17.近几年,我国中东部的大部分地区出现雾霾天气,许多城市的空气质量已经达到了严重污染.下列有关说法中,正确的是( )
| A. | 雾霾天气仅影响出行能见度,对人体健康没有影响 | |
| B. | 减少化石燃料燃烧和汽车尾气排放,是减少雾霾发生的有效措施 | |
| C. | 当光束分别通过雾霾和豆浆时,仅豆浆可看到一条光亮的“通路” | |
| D. | 气候环境报告中新增的“PM2.5”就是雾霾 |
18.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的概念及要求.理想的“原子经济性”反应中,原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放.以下反应中符合“原子经济性”的是( )
| A. | 乙醇催化氧化制乙醛 | B. | 乙醇与浓硫酸共热制乙烯 | ||
| C. | 苯乙烯在一定条件下制聚苯乙烯 | D. | 溴乙烷制乙醇 |
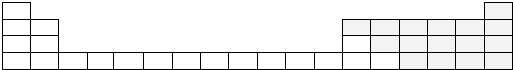
19.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )


| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 原子半径:W>X>Y | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
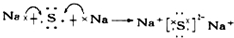 .
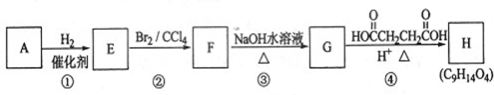
.
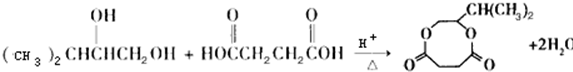 ;
;