题目内容
18.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的概念及要求.理想的“原子经济性”反应中,原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放.以下反应中符合“原子经济性”的是( )| A. | 乙醇催化氧化制乙醛 | B. | 乙醇与浓硫酸共热制乙烯 | ||
| C. | 苯乙烯在一定条件下制聚苯乙烯 | D. | 溴乙烷制乙醇 |
分析 由信息可知,原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放,符合“原子经济性”,则加成反应、加聚反应符合此特点,以此解答该题.
解答 解:A.乙醇催化氧化制乙醛,同时生成水,原子没有全部利用,故A不选;
B.乙醇与浓硫酸共热制乙烯,同时生成水,原子没有全部利用,故B不选;
C.苯乙烯在一定条件下制聚苯乙烯,原料中的原子全部转变成所需要的产物,不产生副产物,实现零排放,故C选;
D.溴乙烷制乙醇,发生水解反应,同时生成HBr,原子没有全部利用,故D不选;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重信息分析及反应类型的考查,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
9.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出大试管中发生反应的化学方程式:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑,该反应是放热反应(填放热或吸热).
(2)实验结果表明,催化剂的催化效果与催化剂接触面积 有关.
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与催化剂接触面积 有关.
6.已知氢气的燃烧热为285.8kJ/mol,CO的燃烧热为282.8kJ/mol;现有氢气和CO组成的混合气体56.0L(标准状况),经充分燃烧后,放出总热量710.0kJ,并生成液态水.下列说法正确的是( )
| A. | CO燃烧的热化学方程为2CO(g)+O2(g)=2CO2(g)△H=+282.8 kJ/mol | |
| B. | H2燃烧的热化学方程为2H2(g)+O2(g)=2H2O(g)△H=-571.6 kJ/mol | |
| C. | 燃烧前混合气体中H2的体积分数为40% | |
| D. | 燃烧后的气体与足量的过氧化钠作用可产生1.50 mol氧气 |
10.部分中学化学常见元素原子结构及性质如表所示:
(1)A原子在周期表中的位置为第四周期Ⅷ族.
(2)B与C形成的化合物的化学式为Mg3N2.
(3)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的水溶液的实验方法是分别取X、Y各少许置于试管中,再各加入少量的MnO2粉末,迅速产生无色气体的是H2O2,无明显现象的是H2O.
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(2)B与C形成的化合物的化学式为Mg3N2.
(3)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的水溶液的实验方法是分别取X、Y各少许置于试管中,再各加入少量的MnO2粉末,迅速产生无色气体的是H2O2,无明显现象的是H2O.
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
7.化学与生活密切相关,下列说法不正确的是( )
| A. | 用热的纯碱溶液可洗涤餐具上的油污 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 用灼烧并闻气味的方法可区别棉麻织物和纯羊毛织物 | |
| D. | 新制Cu(OH)2悬浊液在医院中常用于尿糖的检测 |
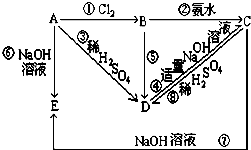 已知A为金属单质,根据下列变化完成以下问题:
已知A为金属单质,根据下列变化完成以下问题: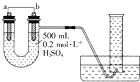 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题: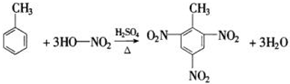
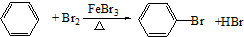
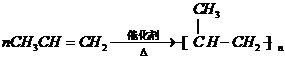
 -CH2CH3+18KMnO4+27H2SO4→5HOOC-
-CH2CH3+18KMnO4+27H2SO4→5HOOC- -COOH+9K2SO4+18MnSO4+5CO2↑+42H2O
-COOH+9K2SO4+18MnSO4+5CO2↑+42H2O