题目内容
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从菜酿性废液(主要會Cu2+、Fe3+、H+、Cl-)中制备氯化亚铜。

(1)操作①②的名称是_________________。
(2)写出加入过量X发生化合反应的离子方程式:____________________。
(3)生成蚀刻液的离子方程式是式:____________________。
(5)写出生成CuCl的化学方程式式:____________________。298K时, Ksp.(CuCl)=1.2×10-6,要使Cu+沉淀完全,则容液中(Cl-)至少为__________________。洗涤CuCl晶体所用的试剂为____(填序号)。
A.饱和Na2CO3溶液 B.NaOH溶液 C.无水乙醇 D.四氯化碳
(5)准确称取所制得的0.250gCuCl样品置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.100mol/L的Ce(SO4)2溶液滴定到终点,消耗22. 60mLCe(SO4)2溶液。已知有关反应的离子方程式为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+;国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.50%。试通过计算说明上述样品是否符合国家标准。_____________________
【答案】 过滤 Fe+2Fe3+=3Fe2+ 2Fe2++Cl2=2Fe3++2Cl- CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4 0.12mol/L C 不符合。
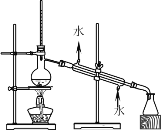
【解析】(1)根据图示操作①的名称是过滤。
(2)因要从废液(主要含Cu2+、Fe3+、H+、Cl-)中制备氯化亚铜。先除杂质H+。向工业上以某酸性废液(含![]() 、
、![]() 、
、![]() 、
、![]() 加入过量的铁粉,三价铁离子与铁粉反应转化为二价铁离子,铜离子与铁反应生成铜, 加入过量X发生化合反应的离子方程式Fe+2Fe3+=3Fe2+ Cu2++Fe=Cu+ Fe2+ 2H++ Fe= Fe2++H2
加入过量的铁粉,三价铁离子与铁粉反应转化为二价铁离子,铜离子与铁反应生成铜, 加入过量X发生化合反应的离子方程式Fe+2Fe3+=3Fe2+ Cu2++Fe=Cu+ Fe2+ 2H++ Fe= Fe2++H2![]()
(3)生成蚀刻液是含有Fe3+的溶液,而溶液中含有大量Fe2+,所以离子方程式是式2Fe2++Cl2=2Fe3++2Cl-
(4)由图 知生成CuCl的化学方程式:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4。
知生成CuCl的化学方程式:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4。
298K时, Ksp.(CuCl)=1.2×10-6,要使C(Cu+)=1![]() 10-5沉淀完全,C(Cl-)=
10-5沉淀完全,C(Cl-)=![]() 带入数值 C(Cl-)= 0.12mol/L。因为氯化亚铜(CuCl)是一种白色粉末,微溶于水不溶于乙醇及稀硫酸。所以洗涤CuCl晶体所用的试剂为无水乙醇。答案:C。
带入数值 C(Cl-)= 0.12mol/L。因为氯化亚铜(CuCl)是一种白色粉末,微溶于水不溶于乙醇及稀硫酸。所以洗涤CuCl晶体所用的试剂为无水乙醇。答案:C。
(5)根据反应:Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+找出关系式
CuCl![]() Fe2+
Fe2+![]() Ce4+
Ce4+
X 0.100mol/L![]() 0.0226L X=2.26
0.0226L X=2.26![]() 10-3 mol
10-3 mol
m(CuCl)= 2.26![]() 10-3 mol
10-3 mol![]() =0.225g
=0.225g
CuCl的质量分数为0.225g/0.250g![]() 100
100![]() =90.00
=90.00![]() <96.50%.所以不符合。
<96.50%.所以不符合。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案