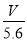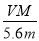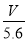题目内容
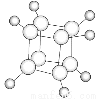
(12分)我国濒临海域的省份,能够充分利用海水制得多种化工产品。如图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中固体B是生活中的一种必需品,E是一种化肥,N是一种常见的金属单质。
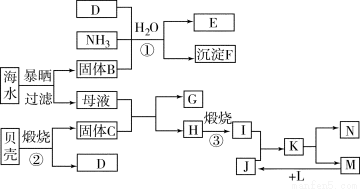
结合上述工艺流程回答下列问题。
(1)物质H和L的化学式分别为 和 。
(2)上述工艺流程中可以循环使用的物质的化学式为____________。
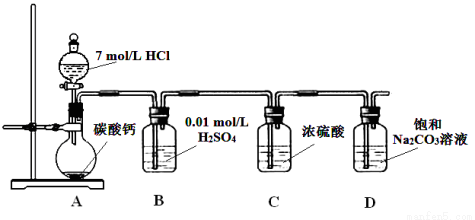
(3)反应①的化学方程式为 ;在反应①中必须先通入NH3,而后通入D,其原因是 。
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为 。
(5)由K溶液经如何处理才能制得N?工业上将K溶液在 的条件蒸发结晶制得无水盐,然后再电解其熔融盐,写出电解的化学反应方程式 。
(1)Mg(OH)2 H2 (2)CO2(各1分)
(3)NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl(2分)
NH3在水中的溶解度大,先通入NH3,有利于吸收CO2(2分)
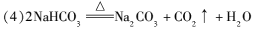 (2分)
(2分)
(5)在氯化氢气流中 (1分) MgCl2 ====Mg + Cl2↑(2分)
【解析】
试题分析:(1)根据题给转化关系知,物质H和L的化学式分别为Mg(OH)2和H2;(2)上述工艺流程中可以循环使用的物质的化学式为CO2。(3)反应①为氨气、氯化钠、二氧化碳和水反应生成碳酸氢钠,化学方程式为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl;在反应①中必须先通入NH3,而后通入D,其原因是NH3在水中的溶解度大,先通入NH3,有利于吸收CO2。(4)工业上利用碳酸氢钠可制得另一种化工产品碳酸钠,该反应的化学方程式为2NaHCO3  Na2CO3 + CO2↑+ H2O。(5)为防止氯化镁水解,工业上将氯化镁溶液在在氯化氢气流中蒸发结晶制得无水盐,然后再电解其熔融盐,电解的化学反应方程式MgCl2
Na2CO3 + CO2↑+ H2O。(5)为防止氯化镁水解,工业上将氯化镁溶液在在氯化氢气流中蒸发结晶制得无水盐,然后再电解其熔融盐,电解的化学反应方程式MgCl2 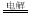 Mg + Cl2↑。
Mg + Cl2↑。
考点:考查无机推断、海水的综合利用。

(14分)硒(34Se)和碲(52Te)都是第VIA族元素,硒是分布在地壳中的稀有元素。工业上硒鼓废料(主要成分硒、碲、碳、铜和铁合金)回收精炼硒的流程如下:
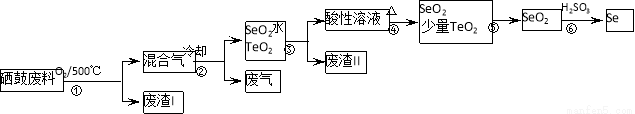
已知:
物理性质 | 熔点 | 沸点 | 升华 | 溶解性 |
SeO2 | 340℃ | 684℃ | 315℃ | 易溶于水 |
TeO2 | 733℃ | 1260℃ | 450℃ | 微溶于水 |
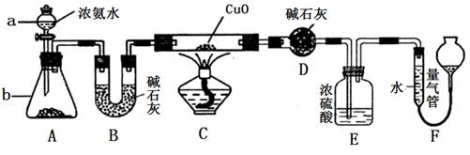
(1)Se的氢化物的电子式是______。
(2)步骤①中通入的氧气使硒鼓废料翻腾,目的是______。
(3)废气的主要成分是______;废渣II的主要成分是______。
(4)步骤④中主要反应的化学方程式是______;步骤⑥反应的化学方程式是______。
(5)根据表中数据,步骤⑤最适宜的分离方法是______。
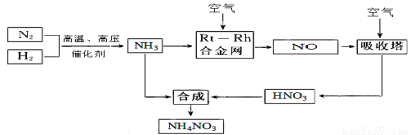
(14分)2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索。“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:①N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = -543kJ·mol-1
②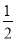 H2(g)+
H2(g)+ 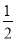 F2(g) = HF(g) △H = -269kJ·mol-1
F2(g) = HF(g) △H = -269kJ·mol-1
③H2(g)+ 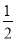 O2(g) = H2O(g) △H = -242kJ·mol-1
O2(g) = H2O(g) △H = -242kJ·mol-1
请写出肼和氟气反应的热化学方程式:_____________________________。
Ⅱ.氧化剂二氧化氮可由NO和 O2生成,已知在2 L密闭容器内,800 ℃时反应:
2NO(g)+O2(g)  2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(1)已知:K800℃>K1000℃,则该反应的ΔH ______0(填“大于”或“小于”),用O2表示从0~2 s内该反应的平均速率为__________。
(2)能说明该反应已达到平衡状态的是________。
A.容器内颜色保持不变 B. 2v逆(NO)=v正(O2)
C.容器内压强保持不变 D.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 。
(4)在上述条件下,计算通入2 mol NO和1 mol O2的平衡常数K=______________。
(5)在上述条件下,若开始通入的是0.2 mol NO2气体,达到化学平衡时,则NO2的转化率为 。