题目内容
【题目】钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化。完成下列计算:
(1)将7.8 g Na2O2完全溶于93.8 g水中,所得溶液中溶质的质量分数为________。
(2)将11.6 g二氧化碳和水蒸气的混合物与足量的Na2O2充分反应,固体质量增加了3.6 g,则原混合气体的平均相对分子质量为________。
(3)向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M(不含结晶水)。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如下图所示。
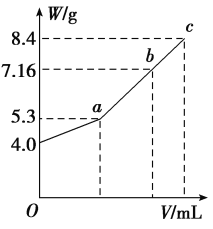
(a)推断b点时M的组成成分_____________________。(填化学式,下同)
(b)若向b点的盐溶液中只加入0.03 mol某钠的化合物,充分反应后,减压低温蒸发得到无水Na2CO3 8.48 g,则加入的物质可以是________或________。
(4)将31 g NaOH和NaHCO3的固体混合物,在密闭容器中加热到250 ℃,经充分反应后排出气体、冷却,称得剩余固体的质量为N g,试分析不同N值时,剩余固体的组成成分(已知NaHCO3的分解温度低于250 ℃)_______________ ________。
【答案】(1)8% (2)23.2 (3)Na2CO3、NaHCO3 Na2O Na2O2
(4)N>26.5时,剩余固体为NaOH和Na2CO3的混合物;N≤26.5时,剩余固体为Na2CO3
【解析】(1)过氧化钠与水反应:
2Na2O2+2H2O===4NaOH + O2↑
156 160 32
7.8 g m(NaOH) m(O2)
解得:m(NaOH)=8 g m(O2)=1.6 g
所得溶液中溶质的质量分数:![]() ×100%=8%。
×100%=8%。
(2)设二氧化碳、水蒸气的物质的量分别是x mol、y mol,则
![]() ,解得
,解得![]() ,所以原混合气体的物质的量为(0.1+0.4)mol=0.5 mol,原混合气体的平均摩尔质量为
,所以原混合气体的物质的量为(0.1+0.4)mol=0.5 mol,原混合气体的平均摩尔质量为![]() =23.2 g/mol。
=23.2 g/mol。
(3)由题图知NaOH质量为4.0 g,物质的量为0.1 mol,完全转化为Na2CO3时,Na2CO3质量为0.1×0.5 mol×106 g/mol=5.3 g,完全转化为NaHCO3时,NaHCO3质量为0.1 mol×84 g/mol=8.4 g,故a点白色固体M为Na2CO3,c点白色固体M为NaHCO3。
(a)b点时M的质量为7.16 g,5.3<7.16<8.4,则M由Na2CO3和NaHCO3组成。
(b)经计算得7.16 g盐中Na2CO3为0.02 mol,NaHCO3为0.06 mol。要得到纯净的8.48 g Na2CO3固体,即要将NaHCO3完全转变为Na2CO3,“则加入的物质”需满足3个条件:a.显碱性或能生成碱,b.含有钠元素,c.不能带来其他杂质。根据钠原子守恒,0.03 mol物质中需有0.06 mol钠原子,故符合条件的有Na2O、Na2O2。
(4)在密闭容器中加热到250 ℃时发生反应:①NaOH+NaHCO3![]() Na2CO3+H2O↑,若碳酸氢钠过量,还发生反应:②2NaHCO3
Na2CO3+H2O↑,若碳酸氢钠过量,还发生反应:②2NaHCO3![]() Na2CO3+CO2↑+H2O↑,若NaOH、NaHCO3恰好按1∶1反应,固体减少质量为水的质量,根据化学方程式可知,生成水的质量为31 g×
Na2CO3+CO2↑+H2O↑,若NaOH、NaHCO3恰好按1∶1反应,固体减少质量为水的质量,根据化学方程式可知,生成水的质量为31 g×![]() =4.5 g,实际固体质量减少(31-N)g,所以当(31-N)g<4.5 g,即N>26.5时说明氢氧化钠过量只发生反应①,最终所得固体为NaOH和Na2CO3的混合物;当(31-N)g>4.5 g,即N<26.5时说明碳酸氢钠过量,发生反应①和②,最终所得固体为Na2CO3;当(31-N)g=4.5 g,即N=26.5 g时只发生反应①,剩余固体为Na2CO3。
=4.5 g,实际固体质量减少(31-N)g,所以当(31-N)g<4.5 g,即N>26.5时说明氢氧化钠过量只发生反应①,最终所得固体为NaOH和Na2CO3的混合物;当(31-N)g>4.5 g,即N<26.5时说明碳酸氢钠过量,发生反应①和②,最终所得固体为Na2CO3;当(31-N)g=4.5 g,即N=26.5 g时只发生反应①,剩余固体为Na2CO3。