题目内容
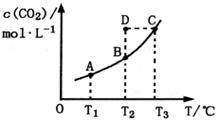
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
 CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH>0 CO2(g)+H2(g)的ΔH>0 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
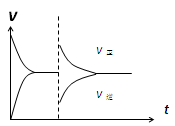
| D.恒压密闭容器中通入1mol CO(g)和1mol H2O(g),发生上述反应,当反应达到平衡后,在其他条件不变时,再通入1mol H2O(g)和1mol CO(g)的混合气体,v正、v逆反应速率随时间t变化的示意图如下。 |

C
根据图像可知,随温度的升高CO2的浓度逐渐增大,说明升高温度平衡向正反应方向移动,即反应是吸热反应,A正确。在T2时D点的浓度大于平衡浓度,因此该点要达到平衡状态,则其浓度一定要减小,所以反应必须向逆反应速率方向移动,B正确。C点比A点温度高,反应物的转化率也高,所以C点反应物的浓度就小,C不正确。要保持恒压,则再加入1mol H2O(g)和1mol CO(g)时,容器的容积必须增大,但由于反应前后体积不变,所以平衡不移动。由于体积增大,导致生成物的浓度减小,反应速率降低,所以选项D是正确的。答案选D。

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
 CO(g)+H2(g), CO(g)+H2O(g)
CO(g)+H2(g), CO(g)+H2O(g)
 3Z B 3X+2Y
3Z B 3X+2Y 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表: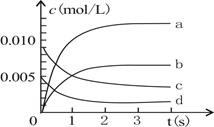
 2AB3(g)(△H<0)平衡体系的是
2AB3(g)(△H<0)平衡体系的是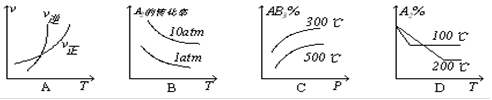

 2NO2(g),△H>0,达平衡时NO的转化率与温度的关系,图上标有A、B、C、D、E点,其中表示未达平衡状态且V正<V逆的点是( )
2NO2(g),△H>0,达平衡时NO的转化率与温度的关系,图上标有A、B、C、D、E点,其中表示未达平衡状态且V正<V逆的点是( )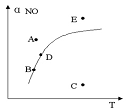
 nC(g)△H>0生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是 ( )
nC(g)△H>0生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是 ( )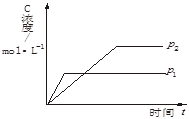
 2NO(g) 能充分说明已达到平衡状态的是( )
2NO(g) 能充分说明已达到平衡状态的是( )