题目内容
【题目】下列实验装置(夹持和尾气处理装置已省略)进行的相应实验,能达到实验目的的是( )
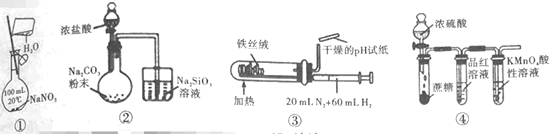
A.利用①装置,配制一定物质的量浓度的NaNO3溶液
B.利用②装置,验证元素的非金属性:Cl>C>Si
C.利用③装置,合成氨并检验氨的生成
D.利用④装置,验证浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
【答案】D
【解析】
A.①装置,不能用容量瓶直接配制溶液,故A错误;
B.②装置,盐酸不是氯元素的最高价含氧酸,盐酸与碳酸钠反应生成二氧化碳不能证明非金属性;通入硅酸钠溶液的气体含有二氧化碳和氯化氢,氯化氢、二氧化碳都能与硅酸钠反应生成沉淀,所以生成硅酸沉淀不能证明非金属性,故B错误;
C.氮气与氢气在铁触媒和高温下生成氨气,氨气遇到干燥的试纸,试纸不能变色,不能达到实验目的,故C错误;
D.浓硫酸具有脱水性、强氧化性,能使蔗糖变黑,反应生成二氧化碳和二氧化硫,二氧化硫具有漂白性可使品红溶液褪色,二氧化硫具有还原性可使酸性高锰酸钾溶液褪色,故D正确;
故选:D。
。

练习册系列答案
相关题目