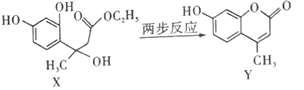
题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1L0.2mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.2NA
B.H2O2+Cl2=2HCl+O2反应中,每生成32gO2,转移2NA个电子
C.3.6gCO和N2的混合气体含质子数为1.8NA
D.常温常压下,30g乙烷气体中所含共价键的数目为7NA
【答案】A
【解析】
A. HCO3在溶液中既能部分电离为CO32-,又部分能水解为H2CO3,故溶液中的 HCO3、CO32-、H2CO3的个数之和为0.1NA,故A错误;
B. 在H2O2+Cl2=2HCl+O2反应中,氧元素由1价变为0价,故生成32g氧气,即1mol氧气时,转移2NA个电子,故B正确;
C. 氮气和CO的摩尔质量均为28g/mol,故3.6g混合物的物质的量为![]() ,又因1个CO和N2分子中两者均含14个质子,故
,又因1个CO和N2分子中两者均含14个质子,故![]() 混合物中含1.8NA个质子,故C正确;
混合物中含1.8NA个质子,故C正确;
D. 常温常压下,30g乙烷的物质的量是1mol,一个乙烷分子有7个共价键,即30g乙烷气体中所含共价键的数目为7NA,故D正确;
故选:A。

练习册系列答案
相关题目