题目内容
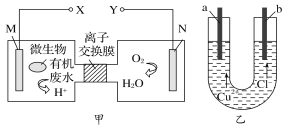
【题目】第二代复合火箭推进剂发生的反应可表示为:①2NH4ClO4→N2↑+Cl2↑+2O2↑+4H2O;②4Al(s)+3O2(g)→2Al2O3(s)+QkJ(Q>0)。完成下列填空:
(1)书写H2O的电子式____________________,Cl原子核外有______种不同能量的电子。
(2)上述物质所形成的晶体中,只包含一种微粒间作用力的是________(填序号)。
a. N2 b. Al2O3 c. H2O d. NH4ClO4
(3)N2和O2都能与H2反应,但二者反应条件差异较大,分析可能原因:①从分子断键角度看,N2分子更难断键,原因是_________________________________;②从原子成键角度看,O原子更易与H原子结合,原因是______________________________________________。
(4)反应①中,氧化产物是_______;生成1molN2时,反应中转移_______NA电子。铵盐都易分解,NH4Cl、NH4HCO4等受热分解得到NH3和相应的酸,而NH4NO3等铵盐和NH4ClO4分解相似,一般无法得到对应酸,且产物可能为N2或NO等物质。请分析不同铵盐受热分解产物存在差异的可能原因:__________。
(5)下列能量变化示意图可与反应②中所体现的能量关系匹配的是________(填序号)。

【答案】![]() 5 b N2分子中存在三键,键能很大 O原子半径更小,吸引电子的能力更强 N2和O2 14 形成铵盐的酸的特性不同 B
5 b N2分子中存在三键,键能很大 O原子半径更小,吸引电子的能力更强 N2和O2 14 形成铵盐的酸的特性不同 B
【解析】
(1)水为共价化合物形成共价键,氯原子核外17个电子,有17种运动状态,不同能量的电子利用电子排布式判断;
(2)晶体中存在微粒间作用力主要有化学键、分子间作用力;
(3)氮气分子中形成氮氮三键,键能大不容易破坏,性质稳定,氧原子原子半径小于氮原子,吸引电子能力强;
(4)反应中元素化合价升高的失电子发生氧化反应得到氧化产物,结合电子守恒计算电子转移总数,铵盐分解生成的酸的稳定性不同,反应得到产物不同;
(5)反应②4Al(s)+3O2(g)=2Al2O3(s)+QkJ(Q>0)是放热反应,反应物能量高于生成物,反应放出的能量是生成物总能量﹣反应物总能量。
(1)水为共价化合物,电子式为:![]() ,氯原子电子排布式为1s22s22p63s23p5,原子核外有5种不同能量的电子;
,氯原子电子排布式为1s22s22p63s23p5,原子核外有5种不同能量的电子;
(2)a.N2存在的微粒间作用力为共价键、分子间作用力,故a不符合;
b.Al2O3 是离子化合物,存在离子键,只包含一种微粒间作用力,故b符合;
c.H2O微粒间存在分子间作用力、共价键,故c不符合;
d.NH4ClO4存在离子键、共价键,故d不符合;
故答案为b;
(3)N2和O2都能与H2反应,但二者反应条件差异较大,分析可能原因:①从分子断键角度看,N2分子更难断键,原因是氮气分子中含有三键,键能大,②从原子成键角度看,O原子更易与H原子结合,原因是氧原子半径小吸引电子的能力强;
(4)①2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O,反应中氮元素化合价﹣3价升高为0价,氧元素化合价﹣2价升高为0价,化合价升高失电子发生氧化反应得到氧化产物,氧化产物是N2、O2,生成1molN2时,反应中转移电子总数为14mol;形成铵盐的酸的特性不同,导致不同酸的铵盐分解产物存在差异。
(5)反应②4Al(s)+3O2(g)=2Al2O3(s)+QkJ(Q>0)是放热反应,反应物能量高于生成物;
A.是吸热反应不符合,故A错误;
B.能量变化表示为反应物能量高于生成物,反应为放热反应,故B正确;
C.反应放出的热量生成物总能量﹣反应物总能量,图象不符合,故C错误;
D.物质能量变化为吸热反应,故D错误;
故答案为B。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案