��Ŀ����
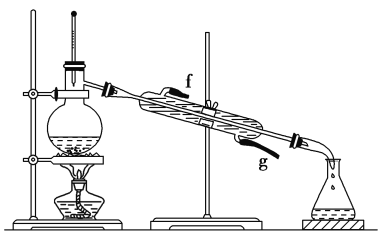
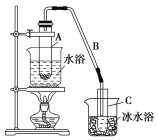
����Ŀ��ijͬѧ���ʵ����̽��Ԫ�����ʵĵݱ���ɣ�ʵ��װ����ͼ��ʾ��
ʵ����������Ԫ����ۺ����������ǿ��̽��Ԫ�طǽ����Եݱ���ɡ�
��֪Aװ�õ���ƿ��װ�д���ʯ����Һ©����װ��ϡHNO3��Bװ����װ�б���̼��������Һ��װ��C��װ��Na2SiO3��Һ���Իش�
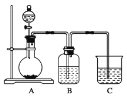
��1��A�з�Ӧ�����ӷ���ʽΪ________________________________________________��C�пɹ۲쵽��������_____________________________________________________��
��2��Bװ�õ�������__________________��
��3������ʵ��������֪̼���衢������Ԫ�طǽ����Ե�ǿ��˳����_____________________��
ʵ��������֪�����¸��������Ũ�����Ͽɲ������������ø�װ��̽���Ⱥ���Ԫ�صķǽ�����ǿ����
��4��д��Bװ���з�����Ӧ�����ӷ���ʽ��________________________________________��
��5��Cװ�õ�������_______________________________________��
��6��ʵ����ۣ������ԣ�_________________���ǽ����ԣ�___________________��
���𰸡�CaCO3+2H+=Ca2++CO2��+H2O ��Һ����� ��ȥ������̼�л��е��������� N��C��Si Cl2��2Br��=Br2��2Cl�� ����β������ֹ��Ⱦ���� Cl2��Br2 Cl��Br
��������
ʵ���Ԫ����ۺ����������ǿ���ж�Ԫ�طǽ�����ǿ��������Խǿ���ǽ�����Խǿ��A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼��֤�����ǽ����Դ���̼��Bװ����Ϊ�����ջӷ�������������������Ӱ��֤��̼�ķǽ����Դ��ڹ��ʵ�飬C��ΪNa2SiO3��Һ��������̼ͨ���������Һ��Ӧ���ɹ��������֤��̼�ķǽ����Դ��ڹ裻
ʵ���̽���ȡ���ķǽ�����ǿ���ĵݱ���ɣ�����ʵ��װ��ͼ��֪��ʵ��ԭ��ΪAװ�ã�Ũ�����������ط�Ӧ��������������ͨ��װ��B���廯����Һ�У���Һ���ֺ�ɫ�����嵥�����ɣ�˵���ȵķǽ�����ǿ���壬װ���лӷ�����������������ж�������Ⱦ����������Ҫ��װ��C������������Һ���ա�
(1)A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼����Ӧ�����ӷ���ʽΪ��CaCO3+2H+=Ca2++CO2��+H2O������ǿ����ȡ�����ԭ�������������ǿ��̼�ᣬ���ᡢ̼��ֱ�ΪN��C����ۺ����ᣬ���Կ�֤�����ǽ����Դ���̼��C��ΪNa2SiO3��Һ��ͨ�������̼��Ӧ���ɹ������������ǿ����ȡ�����ԭ����̼�������ǿ�ڹ��ᣬ̼�ᡢ����ֱ�ΪC. Si����ۺ����ᣬ���Կ�֤��̼�ķǽ����Դ��ڹ裬Cװ���й۲쵽��Һ����ǣ�
(2)�����ӷ�����ȡ�Ķ�����̼�к������ᣬ������ȥ���ᣬ��˵��Cװ���й۲쵽��Һ���������������η�Ӧ������̼������η�Ӧ������Bװ����Ϊ�����ջӷ���������������
(3)A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼��C��ΪNa2SiO3��Һ��ͨ�������̼��Ӧ���ɹ��������֤��̼�������ǿ�ڹ��ᣬ����̼�ᡢ���ᡢ���������ǿ��˳�������ᡢ̼�ᡢ���ᣬ����ʵ�������Ԫ����ۺ����������ǿ���ж�Ԫ�طǽ�����ǿ��������Խǿ���ǽ�����Խǿ����֪C��N��Si����Ԫ�طǽ����Ե�ǿ��ΪN��C��Si��
(4)Aװ�ã�Ũ�����������ط�Ӧ��������2KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2��+8H2O������ͨ��װ��B:�廯����Һ�У�2Br+Cl2Br2+2Cl��Һ���ֺ�ɫ�����嵥�����ɣ�˵���ȵķǽ�����ǿ���壻
(5)װ���лӷ�����������������ж�������Ⱦ���������������������嵥�ʡ�����������Ҫ��װ��C:����������Һ���գ�
(6)���ʵ�������Խǿ����Ԫ�طǽ�����Խǿ�����ݷ�Ӧ��Cl2+2Br�TBr2+2Cl���õ������ԣ�Cl2��Br2���ǽ����ԣ�Cl��Br��

����Ŀ��I. ����ʵ�鷽����������________��
A������������Һ����һ����AgNO3��Һ�У��μӰ�ˮ������ǡ���ܽ�
B���ڼ���ȩ������Cu(OH)2����Һʱ����һ����CuSO4��Һ�У���������NaOH��Һ
C����֤RXΪ����飬��RX���ռ�ˮ��Һ��ϼ��ȣ�����Һ��ȴ���ټ�����������Һ
D����ˮ�Ҵ���Ũ���Ṳ�ȵ�170 �棬���Ƶõ�����ͨ�����Ը�����أ��ɼ����Ƶõ������Ƿ�Ϊ��ϩ
E�������л�����ϩ��ͨ��������һ�������·�Ӧ��ʹ��ϩת��Ϊ����
F����ȥ���ڱ��е��������ӣ����������ˮ������
G��ʵ������ȡ��ϩʱ���뽫�¶ȼƵ�ˮ������뷴ӦҺ�У��ⶨ��ӦҺ���¶�
II.ij��ѧС���������������������װ��(����ͼ)���Ի������Ʊ�����ϩ��
��֪��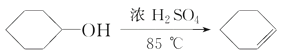 +H2O
+H2O
�ܶ�(g��cm��3) | �۵�(��) | �е�(��) | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
(1)�Ʊ���Ʒ��
��12.5 mL�����������Թ�A�У��ټ���1 mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ��������________________���ڵ���B���˵�������е�������__________��
(2)�Ʊ���Ʒ��
�ٻ���ϩ��Ʒ�к��л������������������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ��________(��ϡ����¡�)�㣬��Һ����______(����)ϴ�ӡ�
a��KMnO4��Һ�� b��ϡH2SO4�� c��Na2CO3��Һ
���ٽ�����ϩ����ͼװ��������ȴˮ��________(�f����g��)�ڽ��롣