题目内容
下列实验装置或操作正确的是 ( )
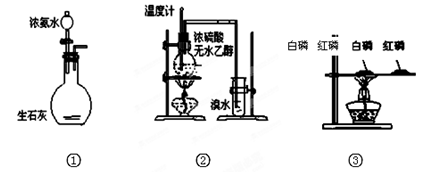


| A.实验① 制取氨气 |
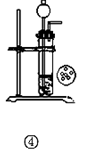
| B.实验② 溴水褪色证明了乙烯可以与溴发生加成反应 |
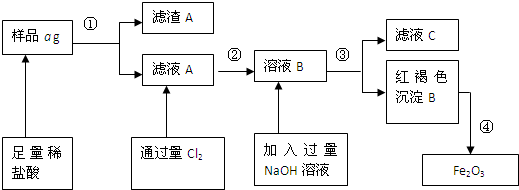
| C.实验③ 比较红磷和白磷的着火点 |
| D.实验④ 用CaC2和饱和食盐水反应制取C2H2 |
A
试题分析:①浓氨水与生石灰可以制取氨气,正确;②乙烯使溴水褪色,不能证明是发生了加成反应,错误;③白磷的温度高,红磷的温度低,但白磷燃烧,红磷不燃烧,不能比较二者的着火点,二者交换位置可以,错误;④碳化钙遇水即成粉末状,所以不能用简易启普发生器装置来控制反应的进行,错误,所以答案选A。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
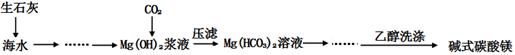
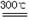 (x+y)MgO+xCO2↑+(y+z)H2O
(x+y)MgO+xCO2↑+(y+z)H2O
 Na2S2O3(aq) (III)
Na2S2O3(aq) (III) =S↓ +SO2↑ +H2O
=S↓ +SO2↑ +H2O


