题目内容
【题目】以某含镍废料(主要成分为NiO,还含有少量FeO、Fe2O3、CoO、SiO2)为原料制备NixOy和碳酸钴的工艺流程如下:
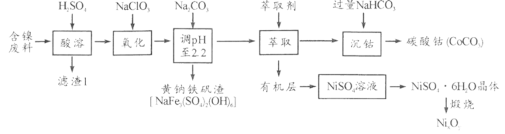
(1)“酸溶”时需将含镍废料粉碎,目的是_________________________________;“滤渣Ⅰ”主要成分为____________________(填化学式)。
(2)“氧化”中添加NaClO3的作用是_______________________,为证明添加NaClO3已足量,可用_______________(写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,其离子方程式为__________________。
(4)“沉钴”过程的离子方程式________________________。若“沉钴”开始时c(Co2+)=0.10 mol/L,则控制pH≤_____________时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15,lg2=0.3)
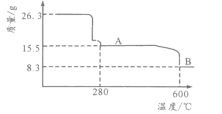
(5)从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,______________,过滤,洗涤,干燥。“煅烧”时剩余固体质量与温度变化曲线如图,该曲线中B段所表示氧化物的化学式为__________________。
【答案】提高浸出率或提高浸出速率(或其他合理答案) SiO2 Fe2+氧化为Fe3+ K3[Fe(CN)6] 3Fe3++Na++2SO42-+3H2O+3CO32-=NaFe3(SO4)3(OH)6↓+3CO2↑ Co2++2HCO3-=CoCO3↓+CO2↑+H2O 7.3 降温结晶(或冷却结晶) Ni2O3
【解析】
金属镍废料(除含 NiO 外,还含有少量 FeO、Fe2O3、CoO等)加入硫酸酸浸,酸浸后的酸性溶液中含有Ni2+、Cl-,另含有少量Fe2+、Fe3+、Co2+等,加入NaClO3氧化亚铁离子为铁离子,加入碳酸钠溶液调节溶液的pH,使铝离子、铁离子全部沉淀,过滤后的滤液中再加入碳酸钠沉淀镍离子得黄钠铁矾渣,滤液中加入萃取剂得到沉钴和有机层,沉钴中加入NaHCO3溶液得碳酸钴;有机层处理后生成NiSO4溶液,蒸发浓缩、冷却结晶、得NiSO4·6H2O晶体,灼烧得NixOy
(1)“酸溶”时需将含镍废料粉碎,目的是提高浸出率或提高浸出速率(或其他合理答案);
“滤渣Ⅰ”主要成分为SiO2(填化学式)。
(2)"氧化"中添加NaClO3的作用是将Fe2+氧化为Fe3+便于除去,为证明添加NaClO3已足量,实际是检验是否含有Fe2+,可用K3[Fe(CN)6]溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,其离子方程式为3Fe3++Na++2SO42-+3H2O+3CO32-=NaFe3(SO4)3(OH)6↓+3CO2↑。
(4)“沉钴”过程的离子方程式Co2++2HCO3-=CoCO3↓+CO2↑+H2O。
若“沉钴”开始时c(Co2+)=0.10 mol/L,Ksp[Co(OH)2]=4.0×10-15=c(Co2+)c2(OH-)=0.10×c2(OH-),c(OH-)=2×10-7,c(H+)=![]() ,pH=-lg
,pH=-lg![]() =7+lg2=7.3,则控制pH≤7.3时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15,lg2=0.3);
=7+lg2=7.3,则控制pH≤7.3时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15,lg2=0.3);
(5)从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,降温结晶(或冷却结晶),过滤,洗涤,干燥。
“煅烧”时剩余固体质量与温度变化曲线如图,从26.3gNiSO4·6H2O失水变成15.5g,n(NiSO4·6H2O):n(H2O)=![]() ,26.3gNiSO4·6H2O中n(Ni)=
,26.3gNiSO4·6H2O中n(Ni)=![]() =0.10mol,8.3g中n(Ni):n(O)=0.1mol:
=0.10mol,8.3g中n(Ni):n(O)=0.1mol:![]() =2:3,该曲线中B段所表示氧化物的化学式为Ni2O3。
=2:3,该曲线中B段所表示氧化物的化学式为Ni2O3。

【题目】下列方案设计能达到实验目的的是
A | B | C | D |
检验淀粉是否水解 | 由褪色快慢研究反应物浓度对反应速率的影响 | 证明发生了取代反应 | 验证Ksp[Cu(OH)2]<Ksp[Mg(OH)2 ] |
|
|
|
|
A.AB.BC.CD.D