题目内容
【题目】 ClO2是一种强氧化性气体,在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图所示装置对其进行制备、收集、吸收并制取NaClO2。

(1)仪器A的名称是________。
(2)图中装置有一明显错误,请指出:________。
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:________。
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:________。
(5)写出一种提高ClO2吸收率的方法:________。
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO2-,当pH≤2时,ClO2-能被I还原。请补充完整检验E装置溶液中存在少量ClO2-的实验方案:取一定体积E装置中的溶液于分液漏斗中,________,则溶液中存在ClO2-。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
【答案】锥形瓶 C装置中导气管应该长进短出 2ClO2+H2O2+2CO32-=2ClO2-+2HCO3-+O2↑ 不能,因为D装置中有氧气产生,氧气也可能将I-氧化为I2 减缓稀硫酸的滴加速率,长导管口加装多孔球泡(其余合理答案) 用CCl4多次萃取、分液,直至溶液中滴加淀粉溶液不显蓝色。向溶液中滴加稀硫酸至溶液的pH≤2,滴加淀粉溶液,溶液变蓝
【解析】
A装置中盛放亚硫酸钠和氯酸钠的固体混合物,当分液漏斗滴加稀硫酸进入A中后,三者混合发生反应生成二氧化氯,C为吸收装置,多余的二氧化氯在装置D中被H2O2和Na2CO3的混合溶液吸收生成NaClO2,装置E检验二氧化氯是否完全被D装置吸收,据此流程进行解答。
(1)根据图示仪器A的名称是锥形瓶;
(2)二氧化氯的密度比空气大,C装置为气体收集装置,应采用向上排空气法,气体应该从长管进短管出,故答案为:C装置中导气管应该长进短出
(3)D中吸收ClO2后生成NaClO2和NaHCO3,ClO2具有强氧化性,化合价降低生成NaClO2,过氧化氢为还原剂,化合价升高生成氧气,化学方程式为:2ClO2+H2O2+2Na2CO3=2NaClO2+2NaHCO3+O2↑,改写成离子方程式为:2ClO2+H2O2+2CO32-=2ClO2-+2HCO3-+O2↑;
(4)E中装有碘化钾溶液出现黄色,说明碘离子被氧化生成了碘单质,但不能说明存在ClO2,因为D中反应生成了氧气,氧气也可能将I氧化为I2,所以出现黄色不能说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,答案为:不能,因为D装置中有氧气产生,氧气也可能将I-氧化为I2;
(5)为提高D中ClO2吸收率,可采取减缓稀硫酸的滴加速率,减慢二氧化氯生成的速率,也可在D中长导管口加装多孔球泡,增大气体与溶液的反应面积等方法,答案为:减缓稀硫酸的滴加速率,长导管口加装多孔球泡;
(6)E装置吸收逸出的少量ClO2气体后所得溶液含有I2和ClO2-,要检验ClO2-必须除去I2,然后调节pH≤2.0再检验,所以检验E装置溶液中存在少量ClO2的实验方案:取一定体积E装置中的溶液于分液漏斗中,用CCl4多次萃取、分液,直至溶液中滴加淀粉溶液不显蓝色。再向溶液中滴加稀硫酸至溶液的pH≤2,滴加淀粉溶液,溶液变蓝,则溶液中存在ClO2-,答案为:用CCl4多次萃取、分液,直至溶液中滴加淀粉溶液不显蓝色。向溶液中滴加稀硫酸至溶液的pH≤2,滴加淀粉溶液,溶液变蓝。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】用50mL0.50mol/L 盐酸与50 mL0.55mol/LNaOH溶液,在右图装置中进行中和热的测定,请回答下列问题:
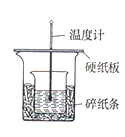
(1)从实验装置看,图中尚缺少的一种玻璃用品是________。
(2)在操作正确的前提下,提高中和热测定准确性的关键是________。
(3)做1次完整的中和热测定实验,温度计需使用________次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?________。
(4)某同学实验记录数据如下表所示假设盐酸和氢氧化钠溶液的密度都是1g/mL,又知中和反应后生成溶液的比热容c=4.18J/(g.℃)根据该同学的实验数据计算,该实验测的中和热△H=________。
温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | |||
HCl | NaOH | ||||
1 | 20.0 | 20.1 | 23.2 | ||
2 | 20.2 | 20.4 | 23.4 | ||
3 | 20.5 | 20.6 | 23.6 | ||