题目内容
8.下列反应不能设计成原电池的是( )| A. | 2CH3OH+3O2→2CO2+4H2O | B. | NaOH+HCl=NaCl+H2O | ||
| C. | Zn+2HCl=ZnCl2+H2↑ | D. | 4Al+3O2+6H2O=4Al(OH)3 |
分析 原电池为将化学能转化为电能的装置,所涉及反应为自发进行的氧化反应,以此解答该题.
解答 解;题中A、C、D为氧化还原反应,且为放热反应,可将化学能转化为电能,而B为中和反应,没有电子的转移,不能形成原电池,
故选B.
点评 本题考查原电池的设计,为高频考点,侧重于学生的分析能力的考查,注意把握原电池的工作原理以及组成条件,难度不大,注意原电池涉及的反应必须是自发进行的氧化还原反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.某元素最高正价氧化物对应的水化物的化学式是HnXOm,该元素的气态氢化物的化学式为( )
| A. | HnX | B. | H(2m-n)X | C. | H(8+n-2m) X | D. | H(8+2m-n) X |
17.下列叙述正确的是( )
| A. | 卤代烃都可发生取代反应 | |
| B. | 由2-氯丙烷制取少量的1,2-丙二醇时,只需要经过取代反应、水解反应 | |
| C. | 实验室制硝基苯时,正确的操作顺序应该是先加入苯,再滴加浓硫酸,最后滴加浓硝酸 | |
| D. | 2-甲基-2-丁烯可以形成顺反异构 |
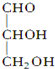
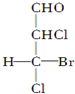

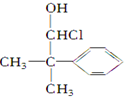
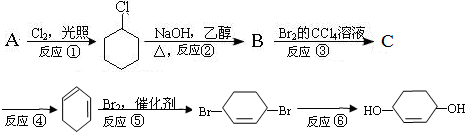
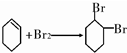
 .
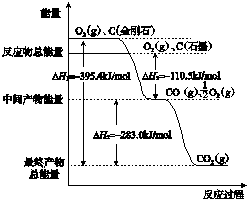
.
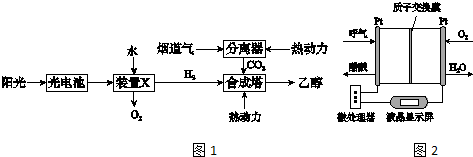
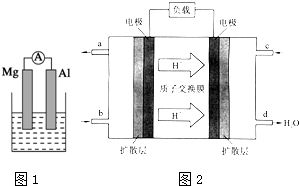 据图回答下列问题:
据图回答下列问题: