题目内容
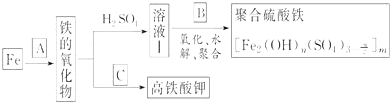
【题目】PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如下图所示。

已知:i.PbCl2微溶于水
ii.PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
(1)浸取过程中MnO2与PbS发生如下反应,请将离子反应补充完整并配平:_____
______+___Cl-+___PbS+___MnO2=___PbCl2+__SO42-+_____ +_____
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是__________。
(3)调pH的目的是____________。
(4)沉降池中获得PbCl2采取的措施有_________。
(5)通过电解酸性废液可重新获得MnO2,装置示意图如下:
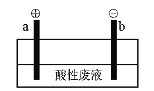
①在_____极(填“a”或“b”)获得MnO2,电极反应为_______________。
②电解过程中发现有Cl2产生,原因可能是_____________(用化学用语表示)。
【答案】8H++2Cl-+PbS+4MnO2=PbCl2+SO42-+4Mn2++4H2O PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq),加入NaCl增大c(Cl-),有利于平衡正向移动,将PbCl2(s)转化为溶液中的离子,消除“钝化层” 除去溶液中的Fe3+ 加水稀释、降温 a Mn2+-2e-+2H2O=MnO2+4H+ 2Cl--2e-=Cl2↑或(MnO2+4HCl=MnCl2+Cl2↑+2H2O)
PbCl42-(aq),加入NaCl增大c(Cl-),有利于平衡正向移动,将PbCl2(s)转化为溶液中的离子,消除“钝化层” 除去溶液中的Fe3+ 加水稀释、降温 a Mn2+-2e-+2H2O=MnO2+4H+ 2Cl--2e-=Cl2↑或(MnO2+4HCl=MnCl2+Cl2↑+2H2O)
【解析】
方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)中加入稀盐酸,根据酸性废液中含有硫酸根离子矿渣,PbS中S元素被氧化成硫酸根离子,则发生反应为4MnO2+PbS+8HCl=3MnCl2+PbCl2+MnSO4+4H2O,加入NaCl促进反应PbCl2(s)+2Cl-(aq)PbCl42-(aq),加入NaOH溶液调节溶液pH,使铁离子转化成氢氧化铁沉淀,过滤得到氢氧化铁、矿渣和滤液;PbCl2微溶于水,将溶液沉降过滤得到PbCl2;电解酸性废液(Mn2+、SO42-、Cl-)可重新获得MnO2,连接电源正极为阳极,发生氧化反应,连接电源负极为阴极,发生还原反应,据此解答。
(1)浸取过程中MnO2与PbS发生反应4MnO2+PbS+8HCl=3MnCl2+PbCl2+MnSO4+4H2O,离子反应为:8H++2Cl-+PbS+4MnO2=PbCl2+4Mn2++SO42-+4H2O;
(2)浸取剂中加入饱和NaCl溶液可有效避免钝化层的原因为:已知PbCl2(s)+2Cl-(aq)PbCl42-(aq),加入NaCl增大c(Cl-),有利于平衡正向移动,将PbCl2(s)转化为溶液中的离子,消除“钝化层”;
(3)根据流程可知调节溶液pH,使铁离子转化成氢氧化铁沉淀,除去溶液中的Fe3+;
(4)已知:PbCl2(s)+2Cl-(aq)PbCl42-(aq)△H>0,可以通过加水稀释、降温促进反应逆向进行,获得PbCl2;
(5)①酸性废液(Mn2+、SO42-、Cl-),得到MnO2,故Mn2+失去电子发生氧化反应得到MnO2,电极反应为:Mn2+-2e-+2H2O=MnO2+4H+,为阳极,则连接a极;
②酸性废液中有氯离子,可能在阳极放电得到氯气,也可能被生成的二氧化锰氧化得到氯气,涉及的反应为:2Cl--2e-=Cl2↑、MnO2+4HCl=MnCl2+Cl2↑+2H2O。

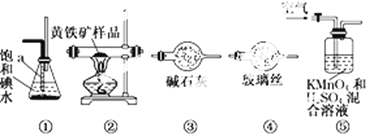
【题目】工业上可用下列仪器组装一套装置来测定黄铁矿(主要成分FeS2)中硫的质量分数(忽略SO2、H2SO3与氧气的反应)。实验的正确操作步骤如下:
A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0 g样品小心地放入硬质玻璃管中
D.以1 L/min的速率鼓入空气
E.将硬质玻璃管中的黄铁矿样品加热到800℃~850℃
F.用300 mL的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O = 2HI+H2SO4
G.吸收液用CCl4萃取、分离
H.取20.00mLG中所得溶液,用0.2000mol·L-1的NaOH标准溶液滴定。试回答:
(1)步骤G中所用主要仪器是______,应取_______ (填“上”或“下”)层溶液进行后续实验。
(2)装置正确的连接顺序是 ![]()
![]()
![]() ④
④ ![]() (填编号)。______
(填编号)。______
(3)装置⑤中高锰酸钾的作用是__________。持续鼓入空气的作用__________。
(4)步骤H中滴定时应选用_____作指示剂,可以根据________现象来判断滴定已经达到终点。
(5)假定黄铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收,滴定得到的数据如下表所示:
滴定次数 | 待测液的体积/mL | NaOH标准溶液的体积/mL | |
滴定前 | 滴定后 | ||
第一次 | 20.00 | 0.00 | 20.48 |
第二次 | 20.00 | 0.22 | 20.20 |
第三次 | 20.00 | 0.36 | 20.38 |
则黄铁矿样品中硫元素的质量分数为___________。
(6)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置①所得吸收液中加入下列哪种试剂__________ 。
A.硝酸银溶液 B.氯化钡溶液 C.澄清石灰水 D.酸性高锰酸钾溶液