题目内容
17.相对分子质量为M的某固体物质在室温下的溶解度为Sg/100g,此时测得饱和溶液的密度为ρg•mL-1,则该饱和溶液的物质的量浓度是$\frac{1000Sρ}{M(100+S)}$mol/L,溶质的质量分数为$\frac{S}{100+S}$×100%.分析 饱和溶液,由溶解度可计算质量分数,密度为ρg•mL-1,再利用c=$\frac{1000ρω}{M}$来计算.
解答 解:在室温下的溶解度为S,此时测得饱和溶液的密度为ρg•mL-1,
溶质的质量分数为$\frac{S}{100+S}$×100%,
由相对分子质量为M,c=$\frac{1000ρω}{M}$,
则c=$\frac{1000Sρ}{M(100+S)}$mol/L.
故答案为:$\frac{1000Sρ}{M(100+S)}$mol/L;$\frac{S}{100+S}$×100%.
点评 本题考查物质的量浓度的计算,侧重于分析、计算能力的考查,熟悉质量分数与饱和溶液的溶解度的关系,质量分数与物质的量浓度的关系即可解答,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.80℃时水的离子积常数KW=3.6×10-13,该温度时纯水的pH值( )
| A. | 等于7 | B. | 小于7? | C. | 大于 | D. | 无法确定 |
9.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol/L NaCl溶液中含有NA个Na+ | |
| B. | 18g H2O中含有NA个H2、NA个O | |
| C. | NA个CCl4分子在标准状况下的体积约为22.4L | |
| D. | 2.3gNa+中含有NA个电子 |
6.下列反应中属于离子反应的有( )
| A. | HCl气体通入硝酸银溶液中 | B. | 碳酸钙固体和稀盐酸制取CO2气体 | ||
| C. | 铁粉和氧气发生反应 | D. | 氯酸钾受热分解制氧气 |
7.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液中加入过量氨水Al3++4NH3 H2O=AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸 CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气 2Fe2++Cl2=2Fe3++2Cl- |
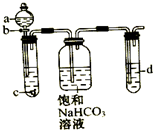 某同学为了探究元素非金属性递变规律,设计了如图所示实验装置.
某同学为了探究元素非金属性递变规律,设计了如图所示实验装置.