题目内容
【题目】铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态铜原子价电子排布式为____________;第二电离能I(Cu)________I (Zn)(填“>”或“<”)。
(2)四氟硼酸四(乙腈)合铜(Ⅰ)配合物是有机合成中常见催化剂,其化学式为[Cu (CH3CN) 4]BF4。
①该配合物中阴离子的空间构型为_____________,与其互为等电子体的分子或离子是______________(各举1例)。
②配体分子中与Cu(I) 形成配位键的原子为____________;配体CH3CN 中的碳原子杂化方式是______。
(3)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,Cu2O 属于____晶体,前者熔点较高,其原因是_______________________________________。
(4)Cu3N 的晶胞(立方)结构如下图所示:
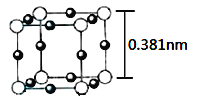
①距离最近的两个Cu+间的距离为________nm;
②Cu3N 晶体的密度为_____________ g·cm-3(列出计算式,不必计算出结果)。
【答案】 3d104s1 > 正四面体 CCl4 、PO43- 、SO42- 、ClO4- N sp、sp3 离子 Cu+离子半径比K+小,晶格能大 ![]()
![]() 或
或![]()
【解析】分析:本题考查物质结构与性质。(1) 基态铜原子核外有29个电子,根据洪特规则分析电子排布式;根据稳定性判断第一电离能I(Cu)>I (Zn)。(2) ①根据中心原子成键电子对数判断空间构型;与其具有相同原子个数和价电子数为等电子体。②N原子有孤电子对,则与Cu(I)形成配位键的原子为N;配体CH3CN中“CN”中碳原子和氮原子形成碳氮三键,则碳原子杂化方式是sp杂化,“—CH3”中碳原子形成4个单键,则碳原子杂化方式是sp3杂化。(3)因Cu+离子半径比K+小,形成的离子键较强,故离子键较强的Cu2O的熔点高。(4)①根据Cu3N的晶胞结构分析;②根据![]() =
=![]() 计算晶胞的密度。
计算晶胞的密度。
详解:(1) 基态铜原子核外有29个电子,根据洪特规则可知,当3d轨道排布10个电子为全充满结构时,原子能量最低,所以基态铜原子价电子排布式为3d104s1;锌原子最外层为4s2全充满结构,比铜最外层4s1稳定,所以第一电离能I(Cu)>I (Zn)。
(2) ①该配合物中阴离子为BF4-,中心B原子价层电子对数为4,孤对电子数为0,则其空间构型为正四面体;与其具有相同原子个数和价电子数的等电子体的分子或离子有CCl4 、PO43- 、SO42- 、ClO4- 等。
②配体分子中C、H原子均没有孤电子对,N原子有孤电子对,则与Cu(I)形成配位键的原子为N;配体CH3CN中“CN”中碳原子和氮原子形成碳氮三键,则碳原子杂化方式是sp杂化,“—CH3”中碳原子形成4个单键,则碳原子杂化方式是sp3杂化。
(3)Cu2O和K2O均属于离子晶体,因Cu+离子半径比K+小,晶格能大,形成的离子键较强,故离子键较强的Cu2O的熔点高。
(4)①根据Cu3N的晶胞结构可知,处于面对角线上的两个Cu+间距离最近,则距离最近的两个Cu+间的距离为![]() ×0.381nm
×0.381nm
②由示意图可知,晶胞中有一个“Cu3N”,一个晶胞质量为:![]() g,一个晶胞体积为
g,一个晶胞体积为
(0.381×10-7)3cm3,晶体密度为 ![]() 或
或![]() g·cm-3。
g·cm-3。

【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2 ![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是
A. 组别①中,0~20min内,NO2的降解速率为0.0125 mol·L-1·min-1
B. 由实验数据可知实验控制的温度T12
C. 40min时,表格中T2应填的数据为0.18
D. 0~10min内,CH4的降解速率①>②
【题目】Ⅰ.乙烯的产量通常用来衡量一个国家的石油化工水平。以乙烯为主要原料合重要的有机化合物路线如下图所示。请回答下列问题。
![]()
(1)A物质所含官能团的名称是____。
(2)反应③的化学方程式是____。
(3)下列物质中,不能通过乙烯加成反应得到的是____(填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
Ⅱ.葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是____。
(2)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是____。
②实验开始时,试管b中的导管不伸入液面下的原因是____。
(3)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水.为研究E的组成与结构,进行了如下实验:
①称取E4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①有机物E的相对分子量为:__. |
②将此9.0gE在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). | ②9.0g有机物E完全燃烧时,经计算:生成CO2共为____ mol. |
③经红外光谱测定,证实其中含有羟基,羧基,甲基 |
④写出E与NaHCO3溶液反应的化学方程式__________。