题目内容
已知N2(g)+3H2(g) 2NH3(g) △H=— 92.4kJ?mo1—1,下列结论正确的是
2NH3(g) △H=— 92.4kJ?mo1—1,下列结论正确的是
 2NH3(g) △H=— 92.4kJ?mo1—1,下列结论正确的是
2NH3(g) △H=— 92.4kJ?mo1—1,下列结论正确的是| A.在密闭容器中加入1mol N2和3mol H2充分反应放热92.4kJ |
B.N2(g)+3H2(g) 2NH3(l)△H=— QkJ?mo1—1,则Q>92.4 2NH3(l)△H=— QkJ?mo1—1,则Q>92.4 |
| C.增大压强,平衡向右移动,平衡常数增大 |
| D.若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率一定为60% |
B
试题分析:A、可逆反应不能进行到底,错误;B、氨气变为液氨放热,正确;C、平衡常数只与温度有关,错误;D、转化率为变化浓度占起始浓度的百分数,N2、H2的变化浓度之比等于1∶3,而起始浓度之比不一定为1∶3,错误。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目

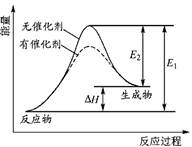


 2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;
2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;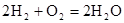 。
。 
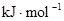
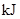
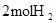 中的化学键
中的化学键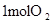 中的化学键
中的化学键 键
键