题目内容
【题目】用于合成树脂的四溴双酚F、药物透过性材料高分子化合物PCL合成如下。
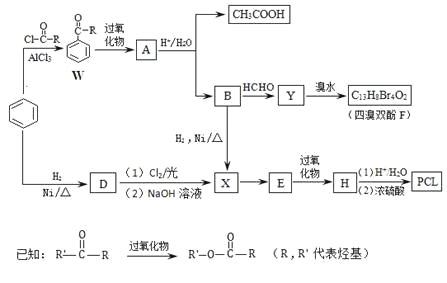
(1)W中—R是_____。
(2)A的结构简式是_________。
(3)A生成B和CH3COOH的反应类型是_________。
(4)D→X过程中所引入的官能团分别是_________。
(5)有机物Y的苯环上只有2种不同化学环境的氢原子。
由Y生成四溴双酚F的反应方程式是________。
【答案】-CH3  取代反应(水解反应) 氯原子(或—Cl)、羟基(—OH)
取代反应(水解反应) 氯原子(或—Cl)、羟基(—OH) 
【解析】
A水解得到乙酸与B,则A属于酯,结合W的结构可知,A为醋酸苯酚酯,即A为![]() ,故W中-R是-CH3,B为
,故W中-R是-CH3,B为![]() .苯与氢气发生加成反应生成D为
.苯与氢气发生加成反应生成D为![]() ,环己烷与氯气发生取代反应,再在氢氧化钠水溶液、加热条件下发生水解反应生成X,而苯酚与氢气发生加成反应也得到X,故X为
,环己烷与氯气发生取代反应,再在氢氧化钠水溶液、加热条件下发生水解反应生成X,而苯酚与氢气发生加成反应也得到X,故X为![]() ,由(5)中E的分子式是C6H10O,E与H2反应可生成X,则X发生催化氧化生成E为
,由(5)中E的分子式是C6H10O,E与H2反应可生成X,则X发生催化氧化生成E为![]() ,结合W到A的转化,可知E与过氧化物反应生成酯,故H为
,结合W到A的转化,可知E与过氧化物反应生成酯,故H为![]() ,H发生水解反应得到HOCH2CH2CH2CH2CH2COOH,再在浓硫酸条件下发生水解反应生成PCL为
,H发生水解反应得到HOCH2CH2CH2CH2CH2COOH,再在浓硫酸条件下发生水解反应生成PCL为![]() .苯酚与甲醛反应得到Y,Y与溴水反应得到四溴双酚F,Y不含Br原子,Y为2分子苯酚与1分子甲醛脱水得到,Y的苯环上只有2种不同化学环境的氢原子,可知2分子苯酚均以对位与甲醛脱水,故Y为
.苯酚与甲醛反应得到Y,Y与溴水反应得到四溴双酚F,Y不含Br原子,Y为2分子苯酚与1分子甲醛脱水得到,Y的苯环上只有2种不同化学环境的氢原子,可知2分子苯酚均以对位与甲醛脱水,故Y为![]() ,F为
,F为 .
.
(1)由上述分析可知,W中-R是-CH3;
(2)由上述分析可知,A的结构简式是![]() ;
;
(3)A生成B和CH3COOH的反应发生酯的水解反应;
(4)D→X过程:![]() 与氯气发生取代反应生成
与氯气发生取代反应生成![]() ,再在氢氧化钠水溶液、加热条件下发生水解反应生成
,再在氢氧化钠水溶液、加热条件下发生水解反应生成![]() ,引入的官能团分别是氯原子、羟基;
,引入的官能团分别是氯原子、羟基;
(5)有机物Y的苯环上只有2种不同化学环境的氢原子,其结构简式为![]() ,生成F的反应为Y与Br2发生的取代反应,反应方程式为:
,生成F的反应为Y与Br2发生的取代反应,反应方程式为:


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】肉桂酸(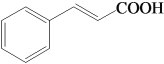 )主要用于香精香料、食品添加剂、有机合成等方面,它的合成原理为
)主要用于香精香料、食品添加剂、有机合成等方面,它的合成原理为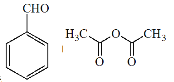
![]()
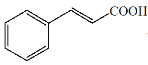 +CH3COOH
+CH3COOH
主要试剂及其物理性质:
名称 | 相对分 子质量 | 性状 | 密度/ (g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解度/(g/100 mL溶剂) | ||
水 | 醇 | 醚 | ||||||
苯甲醛 | 106 | 无色 液体 | 1.044 | -26 | 178~179 | 微溶 | 溶 | 溶 |
乙酸酐 | 102 | 无色 液体 | 1.082 | -73 | 138~140 | 反应 | 溶 | 难溶 |
肉桂酸 | 148 | 白色 粉末 | 1.248 | 133~134 | 300 | 微溶 | 溶 | 溶 |
试剂用量:
试剂名称 | 苯甲醛 | 乙酸酐 | 无水碳酸钾 | 10%氢氧化钠 | 浓盐酸 | 活性炭 |
试剂用量 | 3.0 mL | 5.5 mL | 4~5 g | 40 mL | 25 mL | 1.0 g |
实验仪器如下:
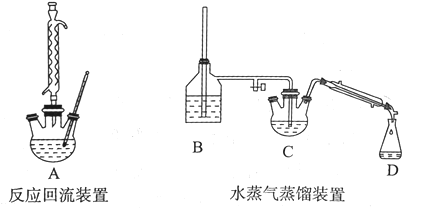
请回答下列问题:
(1)实验准备阶段:在组装实验仪器前要确保反应回流装置彻底干燥,其原因是:_______。
(2)将3.0 mL苯甲醛、5.5 mL乙酸酐和4.00 g无水碳酸钾依次加人250 mL三颈烧瓶中摇匀,烧瓶底部有白色颗粒状固体生成,上部液体无色透明,反应剧烈,有白烟冒出。搭建好回流装置后,开始加热回流。加热回流时控制反应呈微沸状态,加热温度不能太高的原因:_____。
(3)实验结束后,向三颈烧瓶中加人40 mL 10%的氢氧化钠溶液和20 mL的水,可观察到母液体系分为油相和水相。将装置改为水蒸气蒸馏装置,开始加热蒸馏,使油相中的苯甲醛随水蒸气离开母液,开始收集。加人NaOH的作用是:__________。B装置中的长玻璃导管的作用是:_______。水蒸气蒸馏装置中需要加热的仪器有____(填装置序号)。
(4)对蒸气发生器进行加热,待蒸气稳定后再通人烧瓶中的液面下,开始蒸气蒸馏,待检测馏出物中无油滴后停止蒸馏。加人1.0 g活性炭脱色,热过滤。活性炭脱色的原理是______。
(5)加入25 mL的浓盐酸,冰水浴,烧杯中有白色颗粒出现。抽滤(用冰水洗涤),烘箱干燥,称量。称重得m=0.35 g。则该反应的产率约为_____(结果精确至0.1% )。
【题目】(1)根据A~E几种烃分子的结构填空。
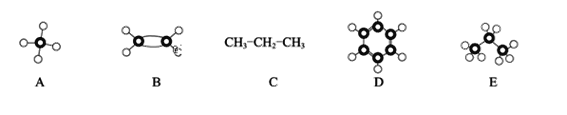
上述分子中属于C的同系物的是_____________(填字母序号)。
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是__________________(填字母序号,下同);
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于________________________;
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是__________。
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:
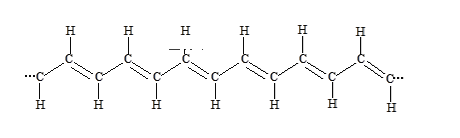
则合成该塑料的单体为___________ (填字母序号,下同);
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是__________;
A 加热分解法 B 电解法 C 高温还原法
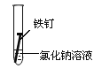
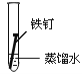
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
实验序号 | A | B | C |
实验 内容 |
|
|
|
一周后,试管中铁钉锈蚀程度最大的是__________;
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过______mol电子。
【题目】下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示:
异丁醇 | 叔丁醇 | |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用蒸馏的方法可将叔丁醇从二者的混合物中分离出来
D. 两种醇发生消去反应后得到同一种烯烃