题目内容
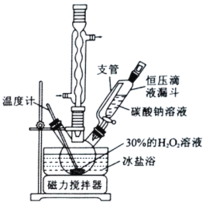
【题目】过氧化尿素[CO(NH2)2·H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如图:
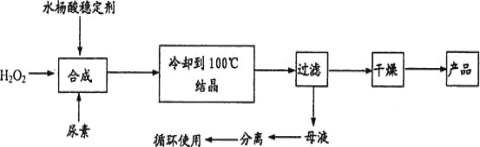
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,其主要原因是____。
(2)从母液中分离出H2O2和尿素,采用的操作是____。
a.盐析、过滤 b.分液、过滤 c.减压蒸馏、结晶 d.常压蒸馏、萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/LKMnO4标准溶液滴定,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①滴定终点的现象是:滴入最后一滴KMnO4溶液后____。
②容量瓶在使用前必须进行的操作是____。
③完成并配平方程式:__MnO4-+___H2O2+___H+=___Mn2++____H2O+____,__
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量___(选填:“偏高”、“偏低”或“不变”)。
⑤根据滴定结果,确定产品中活性氧的质量分数__。
【答案】H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度 c 锥形瓶内溶液显浅红色且半分钟内不褪色 检查是否漏夜 2 5 6 2 8 5O2 偏高 13.3%
【解析】
(1)根据流程,合成过氧化尿素的反应方程式为H2O2+CO(NH2)2 ![]() CO(NH2)2·H2O2,H2O2与尿素的系数比为1:1,因过氧化氢不稳定,受热易分解,因此需要增大过氧化氢的量,提高尿素的利用率或提高过氧化尿素的纯度;
CO(NH2)2·H2O2,H2O2与尿素的系数比为1:1,因过氧化氢不稳定,受热易分解,因此需要增大过氧化氢的量,提高尿素的利用率或提高过氧化尿素的纯度;
答案为H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度;
(2)母液中含有H2O2和尿素,H2O2沸点比尿素低,且H2O2受热易分解,因此从母液中分离出H2O2和尿素,应使溶液在较低温度下蒸发,采用的操作是减压蒸馏,然后结晶,故选项c正确;
答案为c;
(3)①滴定终点的而现象是:滴入最后一滴KMnO4溶液后,锥形瓶内溶液的颜色由无色变为浅紫(红)色且半分钟或30s内不恢复原来颜色;
答案为锥形瓶内溶液的颜色由无色变为浅紫(红)色且半分钟或30s内不恢复原来颜色;
②容量瓶在使用前必须进行的操作是检查是否漏液;
答案为检查是否漏液;
③MnO4-中Mn的化合价又+7→+2价,化合价降低,MnO4-作氧化剂,H2O2作还原剂,H2O2被氧化成O2,H2O2中O由-1价→0价,H2O2整体升高2价,利用化合价升降法进行配平,然后利用原子守恒和离子守恒配平其他,即离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑;
答案为2 5 6 2 8 5O2;
④滴定前滴定管尖嘴处有气泡,滴定后消失,消耗的标准液的体积增大,即会使测得H2O2的含量增大,活性氧含量偏高;
答案为偏高;
⑤高锰酸钾溶液滴定的H2O2,根据得失电子数目守恒,过氧化氢的含量=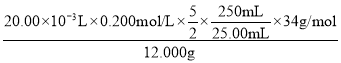 ×100%=28.3%,活性氧16%,相当于H2O234%,则活性氧的含量为13.3%;
×100%=28.3%,活性氧16%,相当于H2O234%,则活性氧的含量为13.3%;
答案为13.3%。

 星级口算天天练系列答案
星级口算天天练系列答案