题目内容
Ⅰ.已知在常温常压下:
① 2CH3OH(l)十3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l)=H2O(g) △H="+" 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如下图:

(1)在Na3PO4溶液中,c(Na+)/c(PO43-) 3(填“>”“=”“<”),向Na3PO4溶液中滴入稀盐酸后 ,pH从10降低到5的过程中发生的主要反应的离子方程式为 。
(2)从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是 。(填选项字母)
A、C(Na+)> C(H2PO4 -)> C(H+)> C(HPO4 2-)> C(H3PO4 )
B、C(Na+)> C(H2PO4 -)> C(OH-)> C( H3PO4)> C(HPO4 2- )
C、C(H+)+ C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4 )
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4 )
(3)假设25℃条件下测得0.1 mol·L–1的Na3PO4溶液的pH=12 ,近似计算出Na3PO4的第一步水解的水解常数Kh(写出计算过程,忽略Na3PO4的第二、第三步水解,结果保留两位有效数字)。
Ⅲ.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染。电化学降解NO3-的原理如图所示。电源正极为 (填A或B),阴极反应式为 。
Ⅰ.CH3OH(g)+3/2 O2(g)= CO2(g)+2H2O(l) △H=-725.8kJ/mol (2分)
Ⅱ.(1)> HPO4 2- + H+= H2PO4 - (每空2分,共4分)
(2)AD(2分)
(3) PO43- + H2O 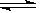 HPO4 2- + OH- (1分)
HPO4 2- + OH- (1分)
起始浓度(mol·L–1): 0.1 0 0
变化浓度(mol·L–1): 0.01 0.01 0.01
平衡浓度(mol·L–1): 0.09 0.01 0.01 (1分)
Kh =C (HPO4 2-)× C(OH-)/ C( PO43- )=0.01 × 0.01 / 0.09 = 1.1 × 10 -3 mol·L–1
Ⅲ. A 2NO3-+10e-+12H+=6H2O +N2↑ (每空2分,共4分)
解析试题分析:Ⅰ.根据已知方程式和盖斯定律,甲醇燃烧的化学方程式为可由(①—②×4)÷2而得,因此表示甲醇燃烧热的热化学方程式为:CH3OH(g)+3/2 O2(g)= CO2(g)+2H2O(l) △H=-725.8kJ/mol。
Ⅱ.(1)Na3PO4溶液中,PO43- 发生水解,因此c(Na+)/c(PO43-)>3,从磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线图可以看出,在pH从10降低到5的过程中,主要是HPO4 2- 的含量在逐渐减小为0,而H2PO4 – 的含量在逐渐增大,因此发生的主要反应的离子方程式为HPO4 2- + H+= H2PO4 - 。
(2)从图中可以看出,H2PO4 – 离子在酸性条件下才能大量存在,因此说明H2PO4 – 的电离大于水解,因此NaH2PO4溶液中有C(HPO4 2-)> C(H3PO4 ),又水电离出的一部分H+ ,因此离子浓度大小顺序有C(Na+)> C(H2PO4 -)> C(H+)> C(HPO4 2-)> C(H3PO4 ),因此A正确;由于H2PO4 – 发生水解和电离后,溶液中含P的微粒有H2PO4-、HPO42- 、PO43-、H3PO4 4种,因此电荷守恒式C错误;物料守恒式D正确。故选AD。
(3)根据溶液水解后的PH=12,可以计算水解产生的c(OH-)=0.01mol/L ,列成三段式有:
PO43- + H2O 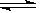 HPO4 2- + OH-
HPO4 2- + OH-
起始浓度(mol·L–1): 0.1 0 0
变化浓度(mol·L–1): 0.01 0.01 0.01
平衡浓度(mol·L–1): 0.09 0.01 0.01
Kh =C (HPO4 2-)× C(OH-)/ C( PO43- )= 0.01 × 0.01 / 0.09 = 1.1 × 10 -3 mol·L–1
Ⅲ.从原理示意图中可以看出,该装置是一个电解池装置,要降解的硝酸盐变成了N2,因此在图中的右侧发生了还原反应,该极为阴极,电源的A极则是正极。阴极反应的方程式为:2NO3-+10e-+12H+=6H2O +N2↑。
考点:本题考查的是燃烧热的热化学方程式的书写、盖斯定律的应用、离子浓度大小比较、水解平衡常数的计算、电化学基础等知识。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即可制冷。该化学物质是 ( )
| A.氯化钠 | B.固体硝酸铵 | C.固体氢氧化钠 | D.生石灰 |
下列反应前后物质的总能量变化可用如图表示的是( )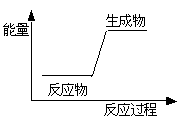
| A.生石灰加水生成熟石灰 |
| B.C+H2O=CO+H2 |
| C.金属钠与水反应 |
| D.HNO3+NaOH=NaNO3+H2O |
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
| A.等质量的O2比O3能量低,由O2变O3为放热反应 |
| B.等质量的O2比O3能量低,由O2变O3 为吸热反应 |
| C.3O2(g)=2O3 (g)△H=285.0 kJ/mol |
| D.O3比O2稳定,由O2变O3 为吸热反应 |
已知反应:①101kPa时,C(s)+ O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol
②稀溶液中:H+(aq)+ OH-(aq )═H2O(l) △H2=-57.3kJ/mol
下列说中正确的是
| A.若碳的燃烧热用△H3表示,则△H3<△H1 |
| B.若碳的燃烧热用△H3来表示,则△H3>△H1 |
| C.浓硫酸与稀NaOH溶液反应的中和热值为57.3kJ·mol-1 |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ的热量 |
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( ) 
| A.该反应为放热反应 |
| B.该反应焓变可表示为△H=-(E1-E2)kJ·mol-1 |
| C.催化剂能降低反应的活化能 |
| D.催化剂能改变反应的焓变 |
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol,
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH=-1135.7kJ/mol,
下列说法正确的是
| A.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-1068 kJ/mol |
| B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4 + H2O=N2H5++ OH- |
| C.铂做电极,以KOH溶液为电解质溶液的肼—空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2↑+4H2O |
| D.铂做电极,以KOH溶液为电解质溶液的肼—空气燃料电池,工作一段时间后,KOH溶液的pH将增大 |
我国二氧化碳的排放量位居世界第二,为减少二氧化碳这种温室气体的排放,下列措施不对的是( )
| A.大力发展氢能源 | B.充分利用太阳能 |
| C.使用含碳能源 | D.提高能源利用率 |