题目内容
9. Na2S2O3俗称大苏打(海波)是重要的化工原料.用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3.已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是Na2S2O3•5H2O.现实验室欲制取Na2S2O3•5H2O晶体(Na2S2O3•5H2O的分子量为248)步骤如下:
Na2S2O3俗称大苏打(海波)是重要的化工原料.用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3.已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是Na2S2O3•5H2O.现实验室欲制取Na2S2O3•5H2O晶体(Na2S2O3•5H2O的分子量为248)步骤如下:①称取12.6g Na2SO3于烧杯中,溶于80.0mL水.
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中.
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤.
④滤液在经过蒸发浓缩、冷却结晶后析出Na2S2O3•5H2O晶体.
⑤进行减压过滤并干燥.
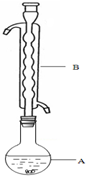
(1)仪器B的名称是球形冷凝管.其作用是冷凝回流.加入的硫粉用乙醇润湿的目的是增加反应物接触面积,提高反应速率.
(2)步骤④应采取的操作是蒸发浓缩、冷却结晶.
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是Na2SO4.如果滤液中该杂质的含量不很低,其检测的方法是:取出少许溶液,加稀盐酸至酸性,静置后,取上层清液或过滤除去S,再加BaCl2溶液,若出现浑浊则含Na2SO4,反之不含.
(4)为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25,00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L 的碘水,用酸式(填“酸式”或“碱式”)滴定管来滴定(2S2O32-+I2=S4O62-+2I-),滴定结果如下:
| 滴定次数 | 滴定前读数(mL) | 滴定滴定后读数(mL) |
| 第一次 | 0.30 | 31.12 |
| 第二次 | 0.36 | 31.56 |
| 第三次 | 1.10 | 31.88 |
分析 (1)根据装置图可知,仪器B为球形冷凝管,结烧瓶中的液体进行冷凝回流,硫粉难溶于水、微溶于乙醇,乙醇湿润可以使硫粉易于分散到溶液中,硫在酒精中微溶,可以增大接触面积,提高反应速率;
(2)溶液中得到溶质固体的方法是通过蒸发浓缩,冷却结晶,过滤洗涤,干燥等步骤得到;
(3)由于S2O32?具有还原性,易被氧气氧化成硫酸根离子可知杂质为硫酸钠,依据硫酸根离子检验方设计实验检验;
(4)碘水有氧化性,能腐蚀橡胶管;依据化学反应方程式2S2O32-+I2═S4O42-+2I-计算即可,测定样品的纯度就是以碘标准溶液为标准的,如果滴定终点没有控制好,碘标准溶液滴加过量也会和亚硫酸钠反应.
解答 解:(1)根据装置图可知,仪器B为球形冷凝管,结烧瓶中的液体进行冷凝回流,硫粉难溶于水微溶于乙醇,所以硫粉在反应前用乙醇湿润是使硫粉易于分散到溶液中,有利于硫粉和Na2SO3溶液充分接触,加快反应速率
故答案为:球形冷凝管;冷凝回流;增加反应物接触面积,提高反应速率;
(2)通过蒸发浓缩,冷却结晶,过滤洗涤,干燥等步骤得到溶液中的溶质固体,
故答案为:蒸发浓缩;冷却结晶;
(3)S2O32?具有还原性,能够被氧气氧化成硫酸根离子,滤液中除Na2S2O3和可能未反应完全的Na2SO3外,存在被氧化产物硫酸钠,所以可能存在的杂质是硫酸钠,其检测的方法依据硫酸根离子检验:取出少许溶液,加盐酸至酸性后,区上层清液或过滤除去S,再加BaCl2溶液.则加入的盐酸发生两个反应的化学方程式为:Na2SO3+2HCl═SO2↑+H2O+2NaCl,Na2S2O3+2HCl=S↓+SO2↑+H2O+2NaCl,取出少许溶液,加稀盐酸至酸性,静置后,取上层清液,再加BaCl2溶液,若出现浑浊则含Na2SO4,反之不含,
故答案为:Na2SO4;取出少许溶液,加稀盐酸至酸性,静置后,取上层清液或过滤除去S,再加BaCl2溶液,若出现浑浊则含Na2SO4,反之不含;
(4)碘水有氧化性,能腐蚀橡胶管,所以碘水应放在酸式滴定管中进行滴定,根据题中表中的数据可知,第二次数据偏差较大,所以取一、三两次实验的数据,所以用去的碘水的体积为$\frac{30.78+30.82}{2}$mL=30.8mL,碘的物质的量为:0.0500mol•L-l×0.0308L=0.00154mol,
2S2O32-+I2═S4O62-+2I-,
2 1
x 0.00154mol
解x=0.00308mol,故Na2S2O3•5H2O的物质的量为0.00308mol,质量为:0.00308×248g/mol=0.7638g,
则称取7.40g产品,配制成250mL溶液中,Na2S2O3•5H2O的质量为=0.7638g×$\frac{250}{25}$=7.638g
故产品的纯度为:$\frac{7.638g}{7.40g}$×100%=103.2%,
碘单质有强的氧化性,Na2SO3具有还原性,Na2SO3会和I2发生反应,从而影响纯度,
故答案为:酸式;103.2%;含有的Na2SO3也会和I2发生反应,从而影响纯度.
点评 本题考查了试剂的作用、物质的推断、滴定的计算、方程式的书写等知识,(4)计算量较大,题目难度较大,注意关系式的应用.

| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 1.0 L 1.0 mol•L-1 的NaAl02水溶液中含有的氧原子数为2 NA? | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 已知C2H4和C3H6混合物的质量为ag,所含原子总数为$\frac{a{N}_{A}}{14}$ |
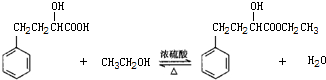
| 相对分子量 | 密度(g/cm3) | 沸点(℃) | 水溶性 | |
| 2-羟基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
| 乙 醇 | 46 | 0.789 | 78.4 | 易溶 |
| 2-羟基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 难溶 |
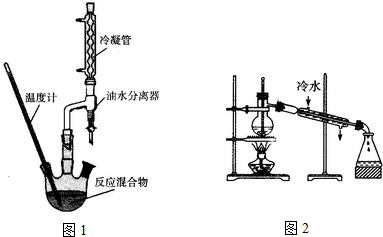
①如图1,在干燥的圆底烧瓶中加入20mL 2-羟基-4-苯基丁酸、20mL无水乙醇和适量浓硫酸,再加入几粒沸石;
②加热至70℃左右保持恒温半小时;
③分离、提纯三颈瓶中的粗产品,得到有机粗产品;
④精制产品.
请回答下列问题:
(1)油水分离器的作用为及时分离产物水,促进平衡向生成酯的反应方向移动
(2)本实验采用水浴加热,因为温度过高会使产率减小(填“增大”、“”减小”或“不变”)
(3)取三颈烧瓶中的混合物分别用水、饱和碳酸氢钠溶液和水洗涤.第二次水洗的目的是洗掉碳酸氢钠
(4)在精制产品时,加入无水MgSO4的作用为干燥;然后过滤,再利用如图2装置进行蒸馏纯化,图2装置中的错误有温度计水银球的位置,冷凝水的方向
(5)若按纠正后的操作进行蒸馏纯化,并收集212℃的馏分,得2-羟基-4-苯基丁酸乙酯约9.0g.则该实验的产率为32%.
| A. | OH- | B. | -NO2 | C. | -COOH | D. | -Cl |
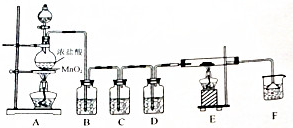 实验室中所用少量氯气用如图装置制取,请回答下列问题:
实验室中所用少量氯气用如图装置制取,请回答下列问题: