��Ŀ����
11��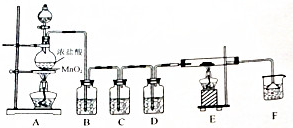 ʵ����������������������ͼװ����ȡ����ش��������⣺
ʵ����������������������ͼװ����ȡ����ش��������⣺��1��д���÷�Ӧ�����ӷ���ʽ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+C12�����ڸ�������ԭ��Ӧ�У�HCl�����������ԡ���ԭ�ԣ�
��2������ƿBʢװ���DZ���ʳ��ˮ��
��3������ƿC��ʢװ����FeCl2��Һ��ʵ�鿪ʼ��C�з�Ӧ�����ӷ���ʽΪ2Fe2++Cl2=2Fe3++2Cl-��ʵ�����п���������ؼ��鷴Ӧ���ɵ������ӣ�
��4������ƿD��ʢװ����ˮ��Eװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������Ϊ������̼���Ȼ��⣬д��E�з�Ӧ�Ļ�ѧ����ʽ��C+2H2O+2Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4HCl��
��5����F������ɫʯ����Һ����ɫ����ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ����ԭ����E�����ɵ������������F�п�ʹ��ɫʯ����Һ��죬��δ��Ӧ�����������F����ˮ��������HClO��HClO����Ư�����ã�ʹ��Һ�ĺ�ɫ��ȥ��
��6������β��ֱ����������У�����Ⱦ������ʵ�����пɲ������������������ж����������÷�Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
���� ��1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ��
���ݷ�Ӧ���Ȼ�������Ԫ�ػ��ϼ۱仯���
��2��Ũ������лӷ��ԣ���ȡ�������к����Ȼ��⣬�����Ȼ��⡢��������ѡ����ʵij��Ӽ����
��3����������ǿ�������ԣ��ܹ����������������������������ӣ��������������������������Ѫ��ɫ��
��4�����������֪��Ӧ��Ϊ̼��ˮ��������������Ϊ������̼���Ȼ��⣻
��5��������ˮ��Ӧ��������ʹ�����������������������ʽ��
��6�������ܹ�������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��� �⣺��1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ�����ӷ���ʽ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+C12����
��ӦMnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+C12�����Ȼ�������Ԫ�ز��ֻ��ϼ����߱���Ϊ��ԭ�ԣ����ֻ��ϼ۲������Ϊ���ԣ�
�ʴ�Ϊ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+C12�������ԡ���ԭ�ԣ�
��2��Ũ������лӷ��ԣ���ȡ�������к����Ȼ��⣬Ҫ��ȡ������������Ӧ��ȥ�Ȼ��⣬�Ȼ���������ˮ�������ڱ���ʳ��ˮ���ܽ�Ȳ������Կ���ѡ��ʳ��ˮ��ȥ�Ȼ��⣬
�ʴ�Ϊ������ʳ��ˮ��
��3����������ǿ�������ԣ��ܹ����������������������������ӣ����ӷ���ʽ��2Fe2++Cl2=2Fe3++2Cl-���������������������������Ѫ��ɫ��������������ؼ������������ӣ�
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��������أ�
��4��Eװ����Ӳ�ʲ�������ʢ��̿�ۣ���E�з���������ԭ��Ӧ�������Ϊ������̼���Ȼ��⣬�ɷ�ӦΪC��HCl��ˮ����Ӧ�ķ���ʽΪC+2H2O+2Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4HCl��
�ʴ�Ϊ��C+2H2O+2Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4HCl��
��5�����ڿ�����Cl2���������Թ�����Cl2��ˮ��������HClO��HClO����Ư�����ã�����ʹF�б��ѱ���ʯ����Һ��ɫ��
�ʴ�Ϊ��E�����ɵ������������F�п�ʹ��ɫʯ����Һ��죬��δ��Ӧ�����������F����ˮ��������HClO��HClO����Ư�����ã�ʹ��Һ�ĺ�ɫ��ȥ��
��6�������ܹ�������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ���������ƣ�Cl2+2OH-=Cl-+ClO-+H2O��
���� �����ۺϿ������������Ʒ������ʡ���ѧʵ�������ʵ��װ�õ����⣬��Ϥ�Ʊ�ԭ���������������ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | ���ᱵ������ˮ���������ᱵ���ǵ���� | |
| B�� | ������̼����ˮ���Ե��磬���Զ�����̼�ǵ���� | |
| C�� | ��̬�����ǵ���ʣ���������������ʱ������ˮʱ���ܵ��� | |
| D�� | Һ̬���ܵ��磬�������ǵ���� |
| ѡ�� | ���ʣ����ʣ� | �Լ� |
| A | ʳ�Σ�ϸɳ�� | NaOH��Һ |
| B | CO��NH3�� | ŨH2SO4 |
| C | CO2��SO2�� | Na2CO3��Һ |
| D | NaHCO3��Һ��Na2CO3�� | Ca��OH��2��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
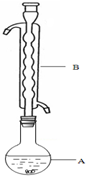 Na2S2O3�׳ƴ��մ���������Ҫ�Ļ���ԭ�ϣ���Na2SO3�������ˮ��Һ�м��ȷ�Ӧ�������Ƶ�Na2S2O3����֪10���70��ʱ��Na2S2O3��100gˮ�е��ܽ�ȷֱ�Ϊ60.0g��212g�������£�����Һ�������ľ�����Na2S2O3•5H2O����ʵ��������ȡNa2S2O3•5H2O���壨Na2S2O3•5H2O�ķ�����Ϊ248���������£�
Na2S2O3�׳ƴ��մ���������Ҫ�Ļ���ԭ�ϣ���Na2SO3�������ˮ��Һ�м��ȷ�Ӧ�������Ƶ�Na2S2O3����֪10���70��ʱ��Na2S2O3��100gˮ�е��ܽ�ȷֱ�Ϊ60.0g��212g�������£�����Һ�������ľ�����Na2S2O3•5H2O����ʵ��������ȡNa2S2O3•5H2O���壨Na2S2O3•5H2O�ķ�����Ϊ248���������£��ٳ�ȡ12.6g Na2SO3���ձ��У�����80.0mLˮ��
����ȡ4.0g��ۣ��������Ҵ���ʪ�ӵ�������Һ�У�
�ۣ���ͼ��ʾ������װ����ȥ����ˮԡ���ȣ��У���ӦԼ1Сʱ����ˣ�
����Һ�ھ�������Ũ������ȴ�ᾧ������Na2S2O3•5H2O���壮
�ݽ��м�ѹ���˲����
��1������B�����������������ܣ������������������������������Ҵ���ʪ��Ŀ�������ӷ�Ӧ��Ӵ��������߷�Ӧ���ʣ�
��2�������Ӧ��ȡ�IJ���������Ũ������ȴ�ᾧ��
��3����Һ�г�Na2S2O3�Ϳ���δ��Ӧ��ȫ��Na2SO3�⣬����ܴ��ڵ���������Na2SO4�������Һ�и����ʵĺ������ܵͣ�����ķ����ǣ�ȡ��������Һ����ϡ���������ԣ����ú�ȡ�ϲ���Һ����˳�ȥS���ټ�BaCl2��Һ�������ֻ�����Na2SO4����֮������
��4��Ϊ�˲��Ʒ�Ĵ��ȣ���ȡ7.40g ��Ʒ�����Ƴ�250mL��Һ������Һ����ȡ25��00mL����ƿ�У��μӵ�����Һ��ָʾ��������Ũ��Ϊ0.0500mol/L �ĵ�ˮ������ʽ�����ʽ����ʽ�����ζ������ζ���2S2O32-+I2=S4O62-+2I-�����ζ�������£�
| �ζ����� | �ζ�ǰ������mL�� | �ζ��ζ��������mL�� |
| ��һ�� | 0.30 | 31.12 |
| �ڶ��� | 0.36 | 31.56 |
| ������ | 1.10 | 31.88 |
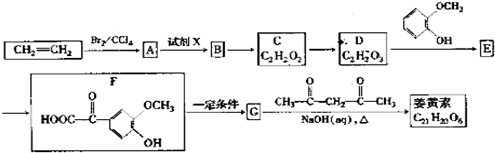

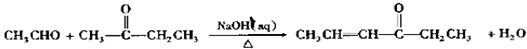

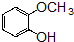 +OHCCOOH��
+OHCCOOH��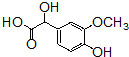 ���䷴Ӧ�����Ǽӳɷ�Ӧ��
���䷴Ӧ�����Ǽӳɷ�Ӧ��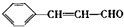 ����д���Ʊ����ȩ�����л���Ľṹ��ʽC6H5CHO��CH3CHO��
����д���Ʊ����ȩ�����л���Ľṹ��ʽC6H5CHO��CH3CHO�� ��E��Ԫ�����ڱ��е�λ�õ�������IA�壮
��E��Ԫ�����ڱ��е�λ�õ�������IA�壮