题目内容
【题目】在如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞的混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极。在A、B中装满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,A、B现象如图所示。请回答下列问题:
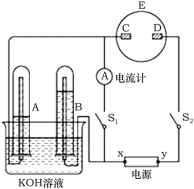
(1)电源负极为________(填“X”或“Y”)。
(2)在滤纸的D端附近,观察到的现象是___________________。
(3)写出电极反应式:B中______________,C中_________________。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1。若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答):
A极_____________________,B极_______________________。
【答案】Y 溶液显红色 4OH--4e-=2H2O+O2↑ 2I--2e-=I2↑ 2H2+4OH--4e-=4H2O 2H2O+O2+4e-=4OH-
【解析】
(1)根据A、B两电极得到的气体体积判断电极名称,从而确定电源X、Y电极名称;
(2)D电极是阴极,溶液中的H+放电,电极反应式是4H++4e-═2H2↑,促进水的电离生成OH-,据此解答;
(3)通直流电,电极A、B及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,所以A极上得氢气,B极上得到氧气;C,D为电解池,C与电源正极相连,为阳极,I-放电生成I2,据此解答;
(4)如果切断S2,闭合S1,则可由A中的H2,B中的O2与KOH溶液形成H2-O2燃料电池,氢气一极是负极,氧气一极是正极,结合守恒思想写出电极反应式;
(1)A、B中充满KOH溶液,切断电源开关S1,闭合开关S2,惰性电极电解KOH溶液,实质就是电解水,所得产物为H2和O2,因为A试管中气体体积是B试管中的2倍,所以A中氢离子得电子生成氢气,电极反应式为4H++4e=2H2↑,B中氢氧根离子失电子生成氧气和水,电极反应式为4OH--4e=2H2O+O2↑,即A为阴极,B为阳极,所以X为正极,Y为负极;
故答案为:Y;
(2)C,D为夹在滤纸两端的铂夹,为电解池,C与电源正极相连,为阳极,D与电源负极相连,为阴极,电极反应为4H++4e-═2H2↑,促进水的电离生成OH-,碱遇酚酞变红;
故答案为:溶液显红色;
(3)惰性电极电解KOH溶液,实质就是电解水,A中为H2,B中为O2,即A为阴极,B为阳极、发生反应4OH--4e-═2H2O+O2↑,C,D为夹在滤纸两端的铂夹,与电源也构成了电解池,C与电源正极相连,为阳极发生反应2I--2e-═I2;
故答案为:4OH--4e-═2H2O+O2↑;2I--2e-═I2;
(4)如果切断S2,闭合S1,则可由A中的H2,B中的O2与KOH溶液形成H2-O2燃料电池,在原电池中氢气一极是负极,电极反应式分2H2+4OH--4e-=4H2O,氧气一极是正极,电极反应式分2H2O+O2+4e-=4OH-;
故答案为:2H2+4OH--4e-=4H2O;2H2O+O2+4e-=4OH-。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中 A 和 F 中装有乙醇和浓硫酸的混合液,D 中的试管里装有液溴。A 中可能存在的副反应有:①乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚。②温度过高产生 CO2(夹持装置已略去)
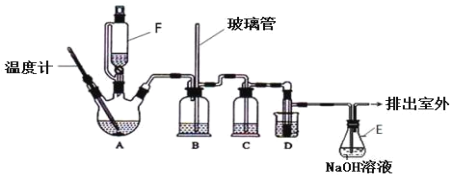
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g· cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
填写下列空白:
(1)A 中发生的主反应的化学方程式:_____;
(2)D 中发生反应的化学方程式为:_____。
(3)安全瓶 B 可以防止倒吸,并可以检查实验进行时导管是否发生堵塞.请写出发生堵塞时瓶 B 中的现象_____。
(4)在装置 C 中应加入_____,其目的是吸收反应中可能生成的酸性气体。
a 水 b 浓硫酸 c 氢氧化钠溶液 d 饱和碳酸氢钠溶液
(5)容器 E 中 NaOH 溶液的作用是_____。
(6)若产物中有少量副产物乙醚,可用_____(填操作名称)的方法除去。
【题目】一定条件下反应:2A(g)+B(g)![]() 3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
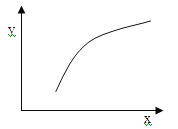
选项 | x | y |
A | A的浓度 | 平衡常数K |
B | 温度 | 混合气体的密度 |
C | B的物质的量 | A的转化率 |
D | 催化剂的质量 | C的体积分数 |
A.AB.BC.CD.D