��Ŀ����
����Ŀ����֪Fe3O4��һ�ָ��ӵĻ�����仯ѧʽ�ɸ�дΪFeO��Fe2O3������A�����ɵĺ�ɫ���ʣ�������ѧϰС����������ֲ�ͬ�IJ��룬������С��ͬѧ���е�ʵ�������̽�����������С���˼·����ʾ�����ؿհס�
�����룩���飺��ɫ������FeO
���飺��ɫ������Fe3O4
���飺_____________��
��ʵ��̽����
(1)������Ϊһ�ּ��Եķ��������жϼ��������ȡA�����ɵĺ�ɫ�����������ձ�����ϡ����ʹ����ȫ�ܽ⣬�ټ�______��Һ�Լ���Fe3�����۲쵽��Һ������_________�����жϡ�
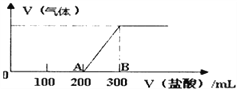
(2)������Ϊ��ͨ�������ⶨ��ȷ��A�����ɵĺ�ɫ���ʵ���ɣ�����֤���������ȷ��ȡA�����ɵĺ�ɫ����2.32g�ܽ�������ϡ�������������ˮ��������ˮ��Ӧ�����ӷ���ʽΪ��_____________���ټ�������NaOH��Һ����ϴ�Ӻ�����ճ��������Ƶù�������Ϊ________�������ж�����ͬѧ������ȷ��
���𰸡���ɫ������FeO��Fe3O4�Ļ���� KSCN ��ɫ 2Fe2++Cl2=2Fe3��+2Cl- 2.4g
��������
Fe����������FeO��Fe2O3��Fe3O4������Fe2O3�Ǻ���ɫ���壬FeO��Fe3O4�Ǻ�ɫ���壻��ɫ������Ϊ���������ΪFeO��Ҳ����ΪFe3O4�����ǻ�����ΪFeO��Fe3O4�Ļ������Ա���ͬѧ�Ʋ�ΪFeO��Fe3O4�Ļ���
(1) Fe3����SCN-���ӣ���Һ��ΪѪ��ɫ����������Һ�м���KSCN��Һ�����۲쵽��Һ������Ѫ��ɫ�����ж���Fe3+����ԭ����ΪFeO��
(2)������������������������Һ��ͨ��Cl2�����������������ԣ�������Һ�е�Fe2+����������ԭ��Ӧ��2Fe2++Cl2=2Fe3��+2Cl-����Ӧ�����Һ�м���������NaOH��Һ������������Ӧ��Fe3++3OH-=Fe(OH)3�������������ˡ�ϴ�ӣ����գ������ֽⷴӦ��2Fe(OH)3![]() Fe2O3+3H2O��������ͬѧ������ȷ����2.32gȫΪFe3O4�������ʵ���Ϊn(Fe3O4)=2.32g��232g/mol=0.01mol������FeԪ���غ㣬�ɵ�n(Fe2O3)=(0.01mol��3)��2=0.015mol���Ƶù�������Ϊm(Fe2O3)=0.015mol��160g/mol=2.4g��
Fe2O3+3H2O��������ͬѧ������ȷ����2.32gȫΪFe3O4�������ʵ���Ϊn(Fe3O4)=2.32g��232g/mol=0.01mol������FeԪ���غ㣬�ɵ�n(Fe2O3)=(0.01mol��3)��2=0.015mol���Ƶù�������Ϊm(Fe2O3)=0.015mol��160g/mol=2.4g��

����Ŀ�����и��������У�X����Ҫ���ʣ�Y���������ʣ�Z��Ϊ��ȥ������Ҫ������Լ������������Լ���ȷ������� (����)
A | B | C | D | |
X | FeCl2��Һ | FeCl3��Һ | Fe | Na2SO4��Һ |
Y | FeCl3 | CuCl2 | Al | Na2CO3 |
Z | Cu | Fe | NaOH��Һ | BaCl2��Һ |
A. A B. B C. C D. D