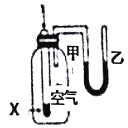题目内容
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+ 3/2O2(g)=C3H3N(g)+3H2O(g) ΔH =-515kJ/mol
①C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ΔH =-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大

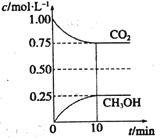
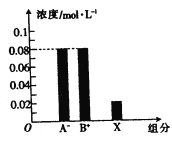
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为,理由是_______________。进料氨、空气、丙烯的理论体积约为________。
【答案】(1)两个反应均为放热量大的反应 降低温度降低压强 催化剂
(2)不是 该反应为放热反应,平衡产率应随温度升高而降低 AC
(3)1 该比例下丙烯腈产率最高,而副产物丙烯醛产率最低 1:7.5:1
【解析】
试题分(1)因为两个反应均为放热量大的反应,所以热力学趋势大;该反应为气体分子数增大的放热反应,所以降低温度、降低压强有利于提高丙烯腈的平衡产率;提高丙烯腈反应选择性的关键因素是催化剂。
(2)因为该反应为放热反应,平衡产率应随温度升高而降低,反应刚开始进行,尚未达到平衡状态,460 ℃以前是建立平衡的过程,所以低于460 ℃时,丙烯腈的产率不是对应温度下的平衡产率;高于460 ℃时,丙烯腈产率降低,A.催化剂在一定温度范围内活性较高,若温度过高,活性降低,正确;B.平衡常数变大,对产率的影响是提高产率才对,错误;C.根据题意,副产物有丙烯醛,副反应增多导致产率下降,正确;D.反应活化能的大小不影响平衡,错误;答案选AC。
(3)根据图像可知,当n(氨)/n(丙烯)约为1时,该比例下丙烯腈产率最高,而副产物丙烯醛产率最低;根据化学反应C3H6(g)+NH3(g)+ 3/2O2(g)=C3H3N(g)+3H2O(g),氨气、氧气、丙烯按1:1.5:1的体积比加入反应达到最佳状态,而空气中氧气约占20%,所以进料氨、空气、丙烯的理论体积约为1:7.5:1。

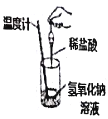
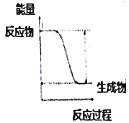
【题目】下列实验现象或图象信息不能充分说明相应化学反应是放热反应的是( )
A | B | C | D | |
反应装置图或图象 |
|
|
|
|
实验现象 | 温度计的水银柱不断上升 | 反应物总能量大于生成物总能量 | 反应开始后,甲处液面低于乙处液面 | 反应开始后,针筒活塞向右移动 |
A. A B. B C. C D. D