题目内容
某校化学研究性学习小组的同学运用实验的手段研究Cu的相关性质。请你参与研究并 回答下列问题:
(1)甲同学取一束细铜丝,用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中。你认为 甲同学在实验中应该观察到的现象是____。
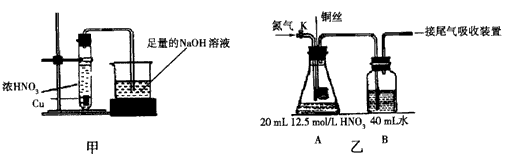
(2)乙同学为验证Cu能和热的浓HNO3反应,设计了如图甲所示的实验,请你指出其中的错误: ___;纠正上述错误后,请你从绿色化学的角度出发,对装置提出改进建议,使装置既能控制反 应的进行,又能减少氮氧化物的排放____。
(1)甲同学取一束细铜丝,用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中。你认为 甲同学在实验中应该观察到的现象是____。
(2)乙同学为验证Cu能和热的浓HNO3反应,设计了如图甲所示的实验,请你指出其中的错误: ___;纠正上述错误后,请你从绿色化学的角度出发,对装置提出改进建议,使装置既能控制反 应的进行,又能减少氮氧化物的排放____。
(3)丙同学在Fe和热的浓HNO3反应后的溶液中加入一块Cu片,Cu片先逐渐溶解,反应一段时间后不再溶解。丙同学依据反应现象:试管上部出现红棕色气体,得出Cu片溶解的原因是Cu 和HNO3发生反应。请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象______。
(4)丁同学探究铜与硝酸反应主要生成NO时对应硝酸的浓度,设计实验装置如图乙所示。(连接好仪器并检查气密性后,分别装入相对应的试剂)
①实验开始前先打开活塞K,持续通入N2一段时间后,关闭K。将铜丝(足量)下移伸入浓硝酸中,有大量的红棕色气体生成,随着反应的进行,气体颜色变浅,当A中充满无色气体时,此时装置A中发生反应的离子方程式为____,接下来的实验操作是____。
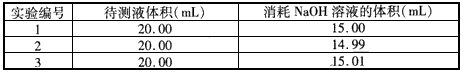
②将B中溶液稀释至200 mL,用0.20 mol/L的NaOH溶液进行滴定。实验数据如下(硝酸的 挥发、分解及体积的变化忽略不计)。则硝酸与铜反应主要生成NO时硝酸的浓度不大于___mol/L,如果在滴定操作时,先俯视 后仰视滴定管读数,所测得的主要生成NO时硝酸的浓度___(“偏大”、“偏小”或“不变”)。
(4)丁同学探究铜与硝酸反应主要生成NO时对应硝酸的浓度,设计实验装置如图乙所示。(连接好仪器并检查气密性后,分别装入相对应的试剂)
①实验开始前先打开活塞K,持续通入N2一段时间后,关闭K。将铜丝(足量)下移伸入浓硝酸中,有大量的红棕色气体生成,随着反应的进行,气体颜色变浅,当A中充满无色气体时,此时装置A中发生反应的离子方程式为____,接下来的实验操作是____。
②将B中溶液稀释至200 mL,用0.20 mol/L的NaOH溶液进行滴定。实验数据如下(硝酸的 挥发、分解及体积的变化忽略不计)。则硝酸与铜反应主要生成NO时硝酸的浓度不大于___mol/L,如果在滴定操作时,先俯视 后仰视滴定管读数,所测得的主要生成NO时硝酸的浓度___(“偏大”、“偏小”或“不变”)。
(1)Cu在Cl2中剧烈燃烧,产生棕黄色烟
(2)试管中液体超过试管容积的三分之一,试管需要加热而应 使其向上倾斜,不应垂直向上;
将装置中的铜片改成一 端为螺旋状的铜丝,螺旋状的一端伸入硝酸中,另一端伸出橡 皮塞
(3)取该溶液少许,滴加适量的KSCN溶液,不出现血红色,再 滴加适量新制氯水,出现血红色
(4)①BCu+8H++ 2NO3-=3Cu2++ 2NO↑+4H2O;将铜丝上提至离开液面,打开K,通入N2一段时间
②8.0;偏小
(2)试管中液体超过试管容积的三分之一,试管需要加热而应 使其向上倾斜,不应垂直向上;
将装置中的铜片改成一 端为螺旋状的铜丝,螺旋状的一端伸入硝酸中,另一端伸出橡 皮塞
(3)取该溶液少许,滴加适量的KSCN溶液,不出现血红色,再 滴加适量新制氯水,出现血红色
(4)①BCu+8H++ 2NO3-=3Cu2++ 2NO↑+4H2O;将铜丝上提至离开液面,打开K,通入N2一段时间
②8.0;偏小

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目

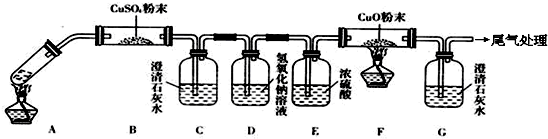
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.