题目内容
用惰性电极电解物质的量浓度相等的CuSO4、NaCl混合溶液,电解过程中不可能发生的反应是
A.2Cl-+Cu2+ Cu+Cl2↑ Cu+Cl2↑ |
B.2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
C.2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
B
解析试题分析:惰性电极电解物质的量浓度相等的CuSO4、NaCl混合溶液可以认为开始电解的是CuCl2,其次是CuSO4和水,最后是水,故B错误。
考点:考查电解有关问题。

练习册系列答案
相关题目
埋在地下的输油铸铁管道,在下列各种情况下被腐蚀速率最慢的是
| A.在潮湿疏松的土壤中 | B.在含铁元素较多的酸性土壤中 |
| C.在干燥致密不透气的土壤中 | D.在含碳较多的潮湿透气的中性土壤中 |
已知空气-锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO+H2O
石墨:O2 + 2H2O + 4e-=4OH- 根据此判断,锌片是:( )
| A.负极,并被还原 | B.负极,并被氧化 |
| C.正极,并被氧化 | D.正极,并被还原 |
有一种氢氧燃料电池以30%KOH溶液为电解质溶液,工作时的电极反应如下:
2H2+4OH-- 4e-=4H2O O2+2H2O+4e-=4OH-,下列说法中错误的是
| A.电池工作时,电子由负极通过外电路流向正极 |
| B.标准状况下,反应3.36L氢气,转移电子0.2mol |
| C.氢氧燃料电池能量利用率高于氢气直接燃烧的能量利用率 |
| D.产物为无污染的水,属于环境友好电池 |
二甲醚是一种绿色、可再生的新能源。如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法不正确的是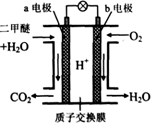
| A.a电极为该电池负极 |
| B.O2在b电极上得电子,被氧化 |
| C.电池工作时,a电极反应式: CH3OCH3—12e-+3H2O→2CO2↑+12H+ |
| D.电池工作时,燃料电池内部H+从a电极移向b电极 |
下列有关金属的说法正确的是
| A.银器在空气中变暗后一定条件下被还原又会变光亮 |
| B.当镀锌铁制品的镀层破损后,镀层不能对铁制品起保护作用 |
| C.不锈钢不生锈是因为表面有保护膜 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
用惰性电极电解200 mLCuSO4溶液。通电一段时间后,测定两极均产生224mL气体(已换算至标准状况下,且忽略溶液体积的变化及气体在溶液中的溶解),则原溶液中溶质的物质的量浓度和所得溶液的pH为
| A.0.04 mol·L-1 1 | B.0.02 mol·L-1 2 |
| C.0.03 mol·L-1 5 | D.0.05 mol·L-1 1 |
如下图所示,甲池的总反应式为:N2H4+O2=N2+2H2O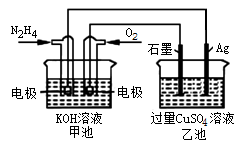
下列关于该电池工作时说法正确的是
| A.甲池中负极反应为:N2H4-4e-=N2+4H+ |
| B.甲池溶液pH不变,乙池溶液pH减小 |
| C.甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
| D.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-=Cl-+2OH-,关于该电池的叙述正确的是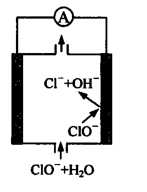
| A.该电池中镁为负极,发生还原反应 |
| B.电池工作时,OH-向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应式为:Mg+ClO-+H2O=Mg(OH)2↓+Cl- |