题目内容
【题目】锌—空气电池是金属空气电池的一种,电解质溶液为KOH溶液时,反应为:2Zn+O2+4OH-+2H2O=2Zn(OH)42-。下列有关说法正确的是
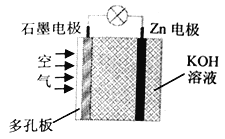
A. 石墨电极上发生氧化反应 B. 正极附近溶液的pH不断减小
C. OH-由锌电极移向石墨电极 D. Zn 电极上发生反应:Zn-2e-+4OH-=Zn(OH)42-
【答案】D
【解析】电池总反应2Zn+O2+4OH-+2H2O=2Zn(OH)42-中Zn元素化合价升高,发生氧化反应,Zn为负极,而氧气中氧元素化合价除低,发生还原反应,通氧气的极为正极;A.石墨电极上通氧气,发生还原反应,故A错误;B.正极附近发生的电极反应为O2+4e-+2H2O=4OH-,则电极周围溶液的pH不断增加,故B错误;C.原电池工作时,OH-向负极Zn移动,故C错误;D.Zn 电极上发生氧化反应,电极反应式为Zn-2e-+4OH-=Zn(OH)42-,故D正确;答案为D。

练习册系列答案
相关题目
【题目】己知:①CO的结构式为C![]() O;②298K时相关化学键的键能数据如下表:
O;②298K时相关化学键的键能数据如下表:
化学键 | H—H | O—H | C—H | C |
E/(KJ·mol-1) | 436 | 465 | 413 | 1076 |
则反应 CO(g)+3H2(g)![]() CH4(g)+H2O(g)的△H的值为
CH4(g)+H2O(g)的△H的值为
A. -198kJ·mol-1 B. +267 kJ·mol-1 C. -298 kJ·mol-1 D. +634 kJ·mol-1

