题目内容
12. A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:(1)A、B、C的第一电离能由小到大的顺序是C<O<N(用对应的元素符号表示);基态D原子的简化电子排布式为[Ar]3d104s1.
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取sp2杂化;BC${\;}_{3}^{-}$的空间构型为平面三角形(用文字描述).
(3)1mol AB-中含有的π键个数为2NA.
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比是1:5.
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力.已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=5(填数值);氢在合金中的密度为0.083g/cm3(请保留小数点后三位).
分析 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大;第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,则A是C元素;C是地壳中含量最多的元素,则C是O元素;B原子的最外层p轨道的电子为半充满结构,且原子序数大于A而小于C,则B是N元素;
D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满,则D是Cu元素;
(1)同一周期元素,元素第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素;
基态D原子核外有29个电子,根据构造原理书写基态D原子的简化电子排布式;
(2)A的最高价氧化物对应的水化物是H2CO3,该分子中中心原子C原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断其中心原子杂化方式及碳酸根离子空间构型;
(3)CN-与N2互为等电子体,则每个CN-中含有2个π键,据此计算1mol CN-中含有的π键个数;
(4)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,利用均摊法计算Ca、Cu原子个数之比;
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,根据Ca、Cu合金确定该镧镍合金中n值;其密度=$\frac{\frac{M}{{N}_{A}}}{V}$.
解答 解:A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大;第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,则A是C元素;C是地壳中含量最多的元素,则C是O元素;B原子的最外层p轨道的电子为半充满结构,且原子序数大于A而小于C,则B是N元素;
D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满,则D是Cu元素;
(1)同一周期元素,元素第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以C、N、O元素第一电离能从小到大顺序是C<O<N;
基态D原子核外有29个电子,根据构造原理书写基态Cu原子的简化电子排布式为[Ar]3d104s1,
故答案为:C<O<N;[Ar]3d104s1;
(2)A的最高价氧化物对应的水化物是H2CO3,该分子中中心原子C原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断其中心原子杂化方式为sp2,碳酸根离子空间构型为平面三角形,
故答案为:sp2;平面三角形;
(3)CN-与N2互为等电子体,则每个CN-中含有2个π键,则1mol CN-中含有的π键个数为2NA,
故答案为:2NA;
(4)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,该晶胞中Ca原子个数=8×$\frac{1}{8}$=1、Cu原子个数=8×$\frac{1}{2}$+1=5,则Ca、Cu原子个数之比为1:5,
故答案为:1:5;
(5)Ca、Cu合金化学式为CaCu5,镧镍合金与上述合金都具有相同类型的晶胞结构XYn,所以该镧镍合金中n=5;
该物质密度=$\frac{\frac{M}{{N}_{A}}}{V}$=$\frac{\frac{4.5}{{N}_{A}}}{9.0×10{\;}^{-23}}$g/cm3=0.083 g/cm3,
故答案为:5;0.083g/cm3.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、原子杂化方式判断、原子核外电子排布等知识点,侧重考查学生分析计算及空间想象能力,难点是晶胞计算,题目难度中等.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案| A. | 向某溶液中加入氨水,产生白色沉淀,证明原溶液中存在Al3+ | |
| B. | 向某溶液中加入NaOH并加热,产生可使湿润红色石蕊试纸变蓝的气体,则原溶液中有NH4+ | |
| C. | 向某溶液中加入Ba(NO3)2溶液,产生白色沉淀,加入稀硝酸沉淀不溶解,则原溶液中有SO42- | |
| D. | 向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl- |
| A. | 同温同压下,体积相同的氢气和氩气所含的分子数相等 | |
| B. | 标准状况下22.4 L乙醇中分子数为NA | |
| C. | 在1 L 2 mol/L的盐酸中,存在2NA个氯化氢分子 | |
| D. | 1.8g的NH4+中含有的电子数为1.1NA |
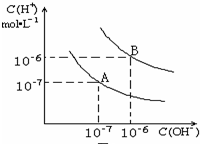 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示:
 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.