题目内容
铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe=FeSO4+Cu
上述两种方法中,铜元素均被__________ (填“氧化”还是“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如下:
①步骤1中反应的离子方程式是_______________。
②步骤2所加的氧化剂最适宜的是____________________。
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到5,此时Fe3+浓度为__________
[Ksp(Fe(OH)3)=4×10-38],可选用的“试剂1”是__________(写出一种即可)。
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是_______________________ (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O。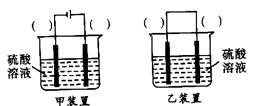
(3)欲实现反应Cu+H2SO4(aq)=CuSO4+H2↑,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)。并写出电极反应式。
27. (15分)(1)还原(2) ①2Fe3++Cu=2Fe2++Cu2+②B
③4×10-11 mol/L CuO[或Cu(OH)2] ④CuCl2在溶液中可以发生水解反应:CuCl2+2H2O Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解
④CuCl2在溶液中可以发生水解反应:CuCl2+2H2O Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解
(3)(3分)如图 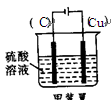 阳极:Cu-2e-=Cu2+ 阴极:2H++2e-=H2
阳极:Cu-2e-=Cu2+ 阴极:2H++2e-=H2
解析试题分析::(1)在火法炼铜:Cu2S+O2=2Cu+SO2和湿法炼铜:CuSO4+Fe═FeSO4+Cu中铜元素的化合价降低,Cu2S、CuSO4都为氧化剂,被还原,发生还原反应,故答案为:还原;
(2)①根据氧化还原反应原理可以写出2Fe3++Cu=2Fe2++Cu2+②由于过氧化氢氧化二价铁离子时不会产生新杂质,故选B。③根据[Ksp(Fe(OH)3)=4×10-38],氢离子浓度为1×10-5 mol/L,代入表达式可求得Fe3+浓度为4×10-11 mol/L。加入 CuO[或Cu(OH)2]不会产生杂质又能调节PH值。④CuCl2在溶液中可以发生水解反应,加入浓盐酸,可以抑制水解,故答案为:CuCl2在溶液中可以发生水解反应,CuCl2+2H2O?Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解;
(3)Cu和H2SO4之间的反应是非自发的,需要电解池实现,金属铜作阳极,阴极是导体即可,电解质为硫酸,即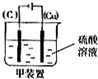 ,故答案
,故答案 .
.
考点:本题考查金属的回收,涉及到氧化还原反应、电解池的工作原理,难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是_______(填序号)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(2)目前已开发出用电解法制取ClO2的新工艺。

①上图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式: 。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_________mol;用平衡移动原理解释阴极区pH增大的原因 。
(3)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含
CN- a mg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为 。
 ClO2↑+___________________(没有配平)
ClO2↑+___________________(没有配平)