题目内容
3.下列化学用语书写正确的是( )| A. | 甲烷的电子式: | B. | 丙烯的键线式: | ||
| C. | 乙醇的结构式: | D. | 乙烯的结构简式:CH2CH2 |
分析 A.甲烷分子中含有4个碳氢键,属于共价化合物,碳原子最外层达到8电子稳定结构;
B.丙烯分子中含有3个C,而 表示的分子中含有4个C,为2-丁烯;
表示的分子中含有4个C,为2-丁烯;
C.乙醇分子中含有官能团羟基,该有机物为二甲醚;
D.乙烯的结构简式中漏掉了官能团碳碳双键.
解答 解:A.甲烷属于共价化合物,分子中存在4个碳氢键,甲烷的电子式为: ,故A正确;
,故A正确;
B.丙烯中含有1个碳碳双键、3个C原子,丙烯的键线式为: ,故B错误;
,故B错误;
C.乙醇分子中含有羟基,其正确的结构式为: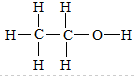 ,故C错误;
,故C错误;
D.乙烯分子中含有碳碳双键,结构简式中应该标出官能团结构,乙烯正确的结构简式为:CH2=CH2,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握键线式、结构简式、结构式、电子式等化学用语的概念及书写原则,明确二甲醚与乙醇的区别,B为易错点,注意确键线式表示的意义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列结论正确的是( )
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | ②⑤⑦ | B. | ②④⑥ | C. | ②④⑤⑥⑦ | D. | ②⑥⑦ |
17.下列化合物中阳离子和阴离子电子层结构相同的是( )
| A. | NaCl | B. | MgF2 | C. | CaF2 | D. | K2O |
11.下列操作会导致实验结果偏高的是( )
| A. | 中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值 | |
| B. | 中和滴定测定盐酸浓度,量取20.00mL盐酸时未用待测液润洗酸式滴定管 | |
| C. | 用托盘天平称量10.5g某物质,砝码和药品的位置放反,所称药品的质量 | |
| D. | 配制一定物质的量浓度溶液时,用量筒量取浓溶液体积仰视读数,所配溶液的浓度 |
18.在下列反应中,HNO3既表现出氧化性,又表现出酸性的是( )
| A. | H2S+2HNO3═S↓+2NO2↑十2H2O | B. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑十O2↑十2H2O | ||
| C. | 3FeO+10HNO3═3Fe(NO3)3十5H2O+NO↑ | D. | CuO+2HNO3═3Cu(NO3)2+H2O |
8.由于碳碳双键不能自由旋转,因此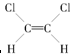 和
和 是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
 和
和 是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |