题目内容
15.既可用来鉴别乙烷和乙烯,又可用来除去乙烷中乙烯得到纯净乙烷的是( )| A. | 通入足量的酸性KMnO4溶液 | B. | 在Ni催化、加热条件下通入H2 | ||
| C. | 通过足量的溴水 | D. | 通过足量的NaOH溶液 |
分析 乙烷性质稳定,与溴水不反应,乙烯含有C=C官能团,能与溴水发生加成反应,注意除杂时不能引入新的杂质且不能影响被提纯的物质.
解答 解:A.乙烯可被氧化生成二氧化碳,引入新杂质,故A错误;
B.通入氢气不能鉴别乙烷和乙烯,且能引入新的杂质,故B错误;
C.乙烷性质稳定,与溴水不反应,乙烯含有C=C官能团,能与溴水发生加成反应生成二溴乙烷而使溴水褪色,故C正确;
D.二者与氢氧化钠溶液都不反应,不能鉴别,故D错误.
故选C.
点评 本题考查物质的鉴别和除杂,为高频考点,题目难度中等,注意乙烯和乙烷在性质上的区别,特别是除杂时要注意不能引入新的杂质.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
5.把一块镁铝合金投入到过量1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示.下列说法中不正确的是( )
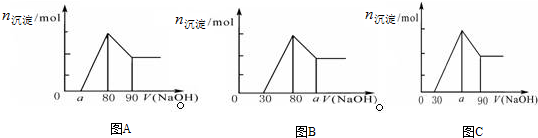

| A. | a的取值范围为 0≤a<50 | |
| B. | $\frac{n(Mg)}{n(Al)}$的最大值为2.5 | |
| C. | 若将关系图改为B图时,则a的取值范围为80<a<90 | |
| D. | 若将关系图改为C图时,则a的取值范围为75<a<90 |
6. 如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )
如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )
 如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )
如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )| A. | CaCl2溶于水时放出热量 | B. | 烧瓶(1)中气体的压强增大 | ||
| C. | NH4Cl溶于水时放出热量 | D. | 烧瓶(3)中气体的压强减小 |
3.下列化合物中,既能发生消去反应,又能发生水解反应的是( )
| A. | 氯仿 | B. | 1-氯甲烷 | C. | 乙醇 | D. | 氯乙烷 |
20.下列指定微粒的个数比为2:1的是( )
| A. | Be2+离子中的质子和电子 | B. | H原子中的中子和质子 | ||
| C. | NaHCO3晶体中的阳离子和阴离子 | D. | Na2O2固体中的阴离子和阳离子 |
7.下列不是海水淡化主要方法的是( )
| A. | 电解法 | B. | 离子交换法 | C. | 电渗析法 | D. | 干馏法 |
4.碱式碳酸铜和氯气都是用途广泛的化工原料.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl-)制备碱式碳酸铜,其制备过程如下:
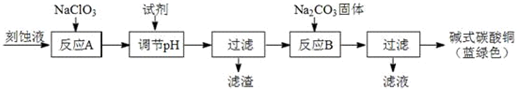
已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
①氯酸钠的作用是将Fe2+氧化成Fe3+并最终除去;
②反应A后调节溶液的pH范围应为3.2-4.2.
③第一次过滤得到的产品洗涤时,如何判断已经洗净?取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
④造成蓝绿色产品中混有CuO杂质的原因是反应B的温度过高.
(2)已知在某温度下Fe(OH)3的容度积常数Ksp=[Fe(OH)3]=1.0×10-38,已知在该温度下溶液中Fe3+离子浓度小于1×10-5mol/L时,该离子已沉淀完全.则该沉淀完全所需要的pH为3.3.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl-)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
②反应A后调节溶液的pH范围应为3.2-4.2.
③第一次过滤得到的产品洗涤时,如何判断已经洗净?取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
④造成蓝绿色产品中混有CuO杂质的原因是反应B的温度过高.
(2)已知在某温度下Fe(OH)3的容度积常数Ksp=[Fe(OH)3]=1.0×10-38,已知在该温度下溶液中Fe3+离子浓度小于1×10-5mol/L时,该离子已沉淀完全.则该沉淀完全所需要的pH为3.3.
 .
.