题目内容
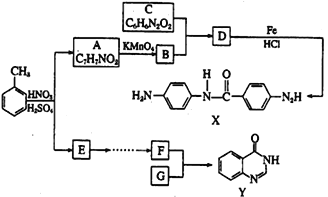
【题目】人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”.试回答下列问题: 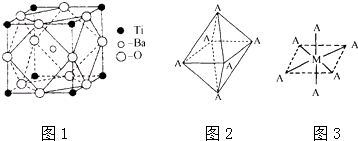
(1)Ti元素在元素周期表中的位置;其基态原子的电子排布式为 .
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定.偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图1所示,它的化学式是 , 其中Ti4+的氧配位数为 , Ba2+的氧配位数为 ,
(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点﹣23.2℃,沸点136.2℃,TiCl4在潮湿空气中易挥发,水解而冒白烟,这是因为水解后有生成.
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图2所示,我们通常可以用下图3所示的方法来表示其空间构型(其中A表示配体,M表示中心原子).配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有种同分异构体.
【答案】
(1)第四周期第四IVB族;[Ar]3d24s2
(2)BaTiO3;6;12
(3)H2TiO3、HC1
(4)2
【解析】解:(1.)根据元素周期表可知Ti元素位于元素周期表的第四周期第ⅣB族,Ti元素是24号元素,根据核外电子排布规律可知,它的基态原子的电子层排布式为:1s22s22p63s23p63d24s2或[Ar]3d24s2 , 所以答案是:第四周期第四IVB族;1s22s22p63s23p63d24s2或[Ar]3d24s2;
(2.)在每个晶胞中均有一个Ba原子,四个Ti原子被四个晶胞共用,每个晶胞中只有一个Ti,12个O原子均被四个晶胞共用,每个晶胞中含有3个O原子,故化学式为BaTiO3 , Ti4+的氧配位数为 ![]() =6,Ba2+的氧配位数为12,所以答案是:BaTiO3;6;12;
=6,Ba2+的氧配位数为12,所以答案是:BaTiO3;6;12;
(3.)TiCl4在潮湿空气中易挥发、水解:TiCl4+3H2O=H2TiO3↓+4HCl,冒白烟,是因为有H2TiO3生成,氯化氢遇水形成盐酸小液滴,呈雾状,
HCl所以答案是:H2TiO3、HC1;
(4.)Co3+位于正八面体的中心,NH3和Cl﹣位于正八面体顶点,当两个Cl﹣相邻时为一种结构,两个Cl﹣不相邻时为另一种结构,共有两种结构,即 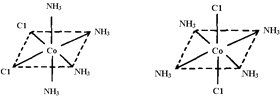 ,所以答案是:2.
,所以答案是:2.

【题目】某化学小组研究盐酸被氧化的条件,进行如下实验.
(1)研究盐酸被MnO2氧化.
实验 | 操作 | 现象 |
I | 常温下将MnO2和12molL-1浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
II | 将 I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
III | 加热MnO2和4molL-1稀盐酸混合物 | 无明显现象 |
①已知MnO2呈弱碱性.I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是______.
②II中发生了分解反应,反应的化学方程式是______.
③III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验(图1)IV进行探究:

将实验 III、IV作对比,得出的结论是______;将 i、ii作对比,得出的结论是______.
④用图2装置(a、b均为石墨电极)进行实验 V:
ⅰ.K闭合时,指针向左偏转
ⅱ.向右管中滴加浓H2SO4至c(H+)≥7molL-1,指针偏转幅度变化不大
ⅲ.再向左管中滴加浓H2SO4至c(H+)≥7molL-1,指针向左偏转幅度增大
将ⅰ和ⅱ、ⅲ作对比,得出的结论是______.
(2)研究盐酸能否被氧化性酸氧化.
①烧瓶中放入浓H2SO4,通过分液漏斗向烧瓶中滴加浓盐酸,烧瓶上方立即产生白雾,用湿润的淀粉KI试纸检验,无明显现象.由此得出浓硫酸______(填“能”或“不能”)氧化盐酸.
②向试管中加入3mL浓盐酸,再加入1mL浓HNO3,试管内液体逐渐变为橙色,加热,产生棕黄色气体,经检验含有NO2.
实验 | 操作 | 现象 |
I | 将湿润的淀粉KI试纸伸入棕黄色气体中 | 试纸先变蓝,后褪色 |
II | 将湿润的淀粉KI试纸伸入纯净Cl2中 | 试纸先变蓝,后褪色 |
III | … | … |
通过实验I、II、III证明混合气体中含有Cl2,III的操作是______.
(3)由上述实验得出:盐酸能否被氧化与氧化剂的种类、______有关.