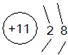题目内容
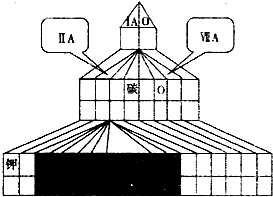
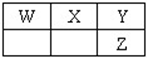 如图是元素周期表主族元素的一部分.短周期元素X的最高正价是+5价,Y单质可在空气中燃烧.下列说法正确的是( )
如图是元素周期表主族元素的一部分.短周期元素X的最高正价是+5价,Y单质可在空气中燃烧.下列说法正确的是( )A、Z的元素符号是S,原子结构示意图为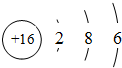 | B、W、X、Y、Z的气态氢化物的稳定性依次减弱 | C、W、X、Y的最高价氧化物对应水化物的酸性依次增强 | D、Y有两种常见的同素异形体,化学式分别为Y2与Y3 |
分析:短周期元素X的最高正价是+5价,则X为第VA族元素,Y为第VIA族元素,Y单质可在空气中燃烧,则Y为S元素,则X为P元素、W为Si元素、Z为Se元素,
A.Z为Se元素,其原子序数是34,核内有34个质子,核外有34个电子;
B.元素的非金属性越强,其气态氢化物的稳定性越强,同一周期元素,元素的非金属性随着原子序数的增大而增强;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期元素,元素的非金属性随着原子序数的增大而增强;
D.Y为S元素,硫的同素异形体有单斜硫和斜方硫.
A.Z为Se元素,其原子序数是34,核内有34个质子,核外有34个电子;
B.元素的非金属性越强,其气态氢化物的稳定性越强,同一周期元素,元素的非金属性随着原子序数的增大而增强;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期元素,元素的非金属性随着原子序数的增大而增强;
D.Y为S元素,硫的同素异形体有单斜硫和斜方硫.
解答:解:短周期元素X的最高正价是+5价,则X为第VA族元素,Y为第VIA族元素,Y单质可在空气中燃烧,则Y为S元素,则X为P元素、W为Si元素、Z为Se元素,
A.Z为Se元素,其原子序数是34,核内有34个质子,核外有34个电子,其原子结构示意图为: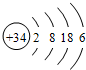 ,故A错误;
,故A错误;
B.W、X、Y元素的非金属性逐渐增强,所以其氢化物的稳定性逐渐增强,故B错误;
C.W、X、Y元素的非金属性逐渐增强,所以其最高价氧化物的水化物酸性逐渐增强,故C正确;
D.Y为S元素,硫的同素异形体S6和S8,故D错误;
故选C.
A.Z为Se元素,其原子序数是34,核内有34个质子,核外有34个电子,其原子结构示意图为:
 ,故A错误;
,故A错误;B.W、X、Y元素的非金属性逐渐增强,所以其氢化物的稳定性逐渐增强,故B错误;
C.W、X、Y元素的非金属性逐渐增强,所以其最高价氧化物的水化物酸性逐渐增强,故C正确;
D.Y为S元素,硫的同素异形体S6和S8,故D错误;
故选C.
点评:本题考查了元素周期表和元素周期律的综合应用,正确推断元素是解本题关键,再结合元素周期律来分析解答,注意该题没有说明Z属于短周期元素,很多同学往往认为Z也属于短周期元素而导致错误,为易错点.

练习册系列答案
相关题目
如图是元素周期表框架
(1)在上面元素周期表中画出主族元素与副族元素的分界线。
(2)下列说法正确的是 。
A.周期表中的主族都有非金属元素 B.周期表中的主族都有金属元素
C.周期表中的非金属元素都位于短周期 D.周期表中的非金属元素都位于主族
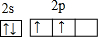
(3)现有甲、乙两种元素,甲元素原子核外2p亚层上有4个电子,乙元素的焰色反应显黄色。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应位置。
② 甲元素与硫元素相比较,非金属性较强的是 (填元素符号),写出可以验证该结论的一个化学反应方程式 。
③ 甲乙两种元素反应可能生成的产物是 。
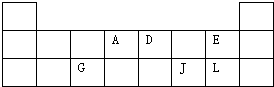 (2010?徐汇区二模)如图为元素周期表的短周期部分.请填空.
(2010?徐汇区二模)如图为元素周期表的短周期部分.请填空.