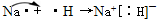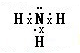题目内容
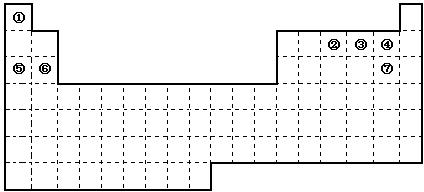
如图是元素周期表框架
(1)在上面元素周期表中画出主族元素与副族元素的分界线。
(2)下列说法正确的是 。
A.周期表中的主族都有非金属元素 B.周期表中的主族都有金属元素
C.周期表中的非金属元素都位于短周期 D.周期表中的非金属元素都位于主族
(3)现有甲、乙两种元素,甲元素原子核外2p亚层上有4个电子,乙元素的焰色反应显黄色。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应位置。
② 甲元素与硫元素相比较,非金属性较强的是 (填元素符号),写出可以验证该结论的一个化学反应方程式 。
③ 甲乙两种元素反应可能生成的产物是 。
(1)如图; (2)D;
|
|
| ||||||||||||||||||||
|
|
| ||||||||||||||||||||
(3)① 如图;
② O; S+O2点燃====SO2;
③ Na2O和Na2O2。
解析:
第(2)小题,应了解非金属元素都在主族,但主族不是都有非金属。其中IA族既有非金属(氢)元素又有金属元素;IIA族全部为金属元素,VIIA族全部为非金属元素,其它也都既有金属元素又有非金属元素。

练习册系列答案
相关题目
如图是元素周期表的框架图,请根据下面提问回答下列问题:
(1)请在表中用实线补全元素周期表的边界.
(2)请用物质的名称填写.
硬度最大的是单质是 ,密度最小的金属是 ;通常状况呈液态的非金属单质是 ,地壳中含量最多的金属元素是 .
(3)在原子序数为1~18号元素中,请用化学式填写.
与水反应最剧烈的金属单质是 ;元素的气态氢化物最稳定的是 ;元素的最高价氧化物所对应的水化物其酸性最强的是 ;原子半径最大的金属与原子半径最小的非金属形成的化合物是 ,并用电子式表示其形成过程: .
(4)在原子序数为1~18号元素中,请按要求填写下列空白.
由两种元素组成的淡黄色化合物的电子式为 ;空气中含量最高的物质的结构式为 ;常温下为气态,固态常用于人工降雨的氧化物的电子式为 ;某元素最高价氧化物的水化物与其气态氢化物反应生成一种盐,该盐的化学式为 ,该化合物中的化学键类型是 .
(2)请用物质的名称填写.
硬度最大的是单质是 ,密度最小的金属是 ;通常状况呈液态的非金属单质是 ,地壳中含量最多的金属元素是 .
(3)在原子序数为1~18号元素中,请用化学式填写.
与水反应最剧烈的金属单质是 ;元素的气态氢化物最稳定的是 ;元素的最高价氧化物所对应的水化物其酸性最强的是 ;原子半径最大的金属与原子半径最小的非金属形成的化合物是 ,并用电子式表示其形成过程: .
(4)在原子序数为1~18号元素中,请按要求填写下列空白.
由两种元素组成的淡黄色化合物的电子式为 ;空气中含量最高的物质的结构式为 ;常温下为气态,固态常用于人工降雨的氧化物的电子式为 ;某元素最高价氧化物的水化物与其气态氢化物反应生成一种盐,该盐的化学式为 ,该化合物中的化学键类型是 .