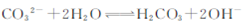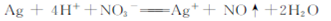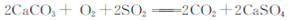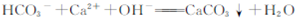题目内容
离子方程式H+ + OH-= H2O可表示的化学方程式是( )
| A.盐酸与氢氧化铜的反应 | B.硫酸氢钠与氢氧化钠的反应 |
| C.硫酸与氢氧化镁的反应 | D.盐酸与氨水的反应 |
B
解析试题分析:A.氢氧化铜难溶于水,不能写成离子形式,错误;B.硫酸氢钠是强酸的酸式盐,拆成离子形式,正确;C.氢氧化镁难溶于水,不能写成离子形式,错误;D.氨水中的一水合氨是弱电解质,不能写成离子形式,错误。
考点:考查化学反应的离子方程式的表示形式的知识。

练习册系列答案
相关题目
室温下,下列各组离子能大量共存的是
| A.稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| B.Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
C.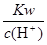 =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- |
| D.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
下列指定反应的离子方程式正确的是
| A.Cu溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
溶液中含有HCO 、SO
、SO 、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
A.HCO | B.SO | C.Cl- | D.Na+ |
下列各环境下的离子组合一定能大量共存的是( )
| A.c(HCO3-)=1×10-1mol/L的溶液中Na+、AlO2-、CH3COO-、K+ |
| B.由水电离出的c(H+)=1×10-14mol/L的溶液中CO32-、NH4+、SO42-、K+ |
| C.甲基橙呈红色的溶液中Fe2+、Cl-、NO3-、Na+ |
| D.能使pH试纸呈红色的溶液中Mg2+、Cl-、NO3-、SO42- |
下列离子方程式书写正确的是
| A.Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.Fe与FeCl3溶液反应:Fe+Fe3+=2Fe2+ |
| C.大理石中加入稀盐酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.AlCl3溶液中加过量氨水:Al3++3OH-=Al(OH)3↓ |
在无色溶液中,下列离子能大量共存的是
| A.Na+、NH4+、NO3-、MnO4- | B.Mg2+、SO42-、K +、Cl- |
| C.K +、Cu2+ 、Cl-、Br- | D.Ba2+ 、Na+ 、OH-、HCO3- |