题目内容
【题目】0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是
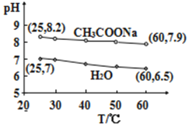
A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
【答案】D
【解析】
A.从图中可以看出,25℃时CH3COONa溶液的pH=8.2,大于纯水的pH,所以溶液显碱性,A正确;
B.60℃,水的电离程度比25℃时大,但H2O中c(H+)= c(OH-),所以溶液呈中性,B正确;
C.60℃,水的离子积常数KW=10-13(mol/L)2,CH3COONa溶液中c(OH-)=![]() =1×10-5.1mol·L-1,C正确;
=1×10-5.1mol·L-1,C正确;
D.CH3COO-的水解是一个吸热过程,升高温度,CH3COONa溶液水解程度增大,D错误;
故选D。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目