题目内容
下列常用实验室仪器中,一般不用于混合物分离或提纯的是
A.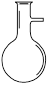 | B.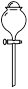 | C.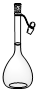 | D. |
C
试题分析:一般用于混合物分离或提纯的操作是过滤、蒸馏、萃取或分液,常用的仪器分别是漏斗、蒸馏烧瓶、分液漏斗。根据装置特点可知,A~D分别是蒸馏烧瓶、分液漏斗、容量瓶和漏斗。容量瓶常用来配制一定物质的量浓度,不用于物质的分离和提纯,因此正确的答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
题目内容
A.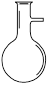 | B.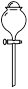 | C.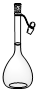 | D. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案