题目内容
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使甲基橙变黄色的溶液中:Na+、Al3+、![]() 、Cl-
、Cl-
B.0.1mol/L的烧碱溶液中:K+、Ba2+、Cl-、HCO3-
C.![]() =1×10-13 mol·L-1的溶液中:
=1×10-13 mol·L-1的溶液中:![]() 、Ca2+、Cl-、
、Ca2+、Cl-、![]()
D.水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、![]() 、
、![]()
【答案】C
【解析】
A.使甲基橙变黄色的溶液的pH>4.4,溶液可能为碱性,Al3+与氢氧根离子反应,在溶液中不能大量共存,A不符合题意;
B.烧碱就是氢氧化钠,0.1mol/L的烧碱溶液显碱性,氢氧根离子与HCO3-发生反应,在溶液中不能大量共存,B不符合题意;
C.常温下,![]() =1×10-13mol/L即
=1×10-13mol/L即![]() = c(OH-)=1×10-13mol/L,所以c(H+)=10-1mol/L,溶液显酸性,NH4+、Ca2+、Cl-、NO3-相互间不会发生反应,可以大量共存,C符合题意;
= c(OH-)=1×10-13mol/L,所以c(H+)=10-1mol/L,溶液显酸性,NH4+、Ca2+、Cl-、NO3-相互间不会发生反应,可以大量共存,C符合题意; ![]()
D.水电离的c(H+)=1×10-13mol·L-1,说明水的电离受到了抑制,溶液可能显酸性,也可能显碱性,酸性溶液中H+能与AlO2-、CO32-发生反应,不能大量共存,D不符合题意;
答案选C 。

 阅读快车系列答案
阅读快车系列答案【题目】磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
物质 | H3PO4 | HF |
电离常数 | Ka1=7.1×103; Ka2=6.3×108; Ka3=4.2×1013 | Ka=6.6×104 |
向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为____________
(2)已知:
Ⅰ.CaO(s)+H2SO4(l)![]() CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)![]() Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为____________。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率________(填“增大”“减小”或“不变”,下同);HF的平衡浓度________。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH。
CO2(g)+H2(g) ΔH。
①一定温度下,向10L密闭容器中充入0.5mol CO和1mol H2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02mol·L1·min1。则CO的平衡转化率α=________;该反应的平衡常数K=________。
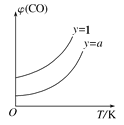
②在压强不变的密闭容器中发生上述反应,设起始的![]() =y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由为_____________
=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由为_____________
【题目】某同学利用下图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )
X气体 | Y试剂 | Z试剂 | |
A. | NO2 | H2O | H2O |
B. | CO2 | H2O | H2O |
C. | HCl | 饱和食盐水 | 水 |
D. | NO2 和O2 | H2O | H2O |
A.AB.BC.CD.D