��Ŀ����
����Ŀ����ʽ������[Fe(OH)SO4]��������ˮ����ýȾ���ȡ���ҵ�����÷���м(����������������������)������ʽ�������IJ��ֹ������£�
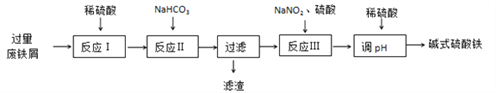
��֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
��ʼ���� | 2.3 | 7.5 | 3.4 |
��ȫ���� | 3.2 | 9.7 | 4.4 |
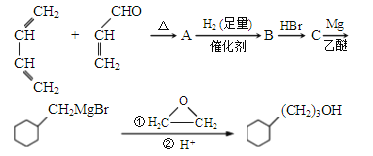
(1)��Ӧ����������ԭ��Ӧ�����ӷ���ʽ__________________ �� __________________��
(2)��Ӧ���м���NaHCO3������ϵ��pH��_____________��Χ�ڡ�
(3)��Ӧ�������ɵ����������������ɫ���÷�Ӧ�����ӷ���ʽ��_________________��
(4)����Ӧ����ͨ��O2�ɼ���NaNO2��������������1molO2�ɽ�Լn(NaNO2)=____mol��
(5)��ʽ����������ˮ�����ɵ�Fe(OH)2+���ӿɲ���ˮ������Fe2(OH)42+ �ۺ����ӣ���ˮ�ⷴӦ�����ӷ���ʽΪ____________________________
���𰸡� Fe +H+ ��Fe2+ + H2 �� Fe +2 Fe3+��3Fe2+ 4.4��pH<7.5 Fe2+ + NO2- +2H+ ��Fe3++ NO ��+H2O 4 2Fe��OH��2+ + 2H2O![]() Fe2��OH��42+ + 2H+
Fe2��OH��42+ + 2H+
�����������⿼�黯ѧ�������̣���1������м�к���Fe��Fe2O3��Al2O3����ӦI�м���ϡ���ᣬ����Al2O3��6H��=2Al3����3H2O��Fe2O3��6H��=2Fe3����3H2O��Fe��2Fe3��=3Fe2����Fe��2H��=Fe2����H2��������������ԭ��Ӧ�����ӷ���ʽΪFe��2Fe3��=3Fe2����Fe��2H��=Fe2����H2��������̼�����Ƶ�Ŀ���dz�ȥ����Al3�������pH���ڷ�Χ��4.4��pH<7.5����3�����ɵ����������������ɫ��˵�����ɵ�����ΪNO����������������������Fe2��������Fe3������������ԭΪNO�����ӷ�Ӧ����ʽΪ��Fe2�� + NO2�� +2H�� ��Fe3��+ NO ��+H2O����4��1molO2���뷴Ӧ���õ�4mol���ӣ��õ�4mol���ӣ���Ҫ����NaNO2�����ʵ���Ϊ4/1mol=4mol����5��������Ϣ���ó���2Fe��OH��2+ + 2H2O![]() Fe2��OH��42+ + 2H����
Fe2��OH��42+ + 2H����

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�����Ŀ������ʵ����ʵ�ó�����Ӧ���۲���ȷ����
ѡ�� | ��ʵ | ���� |
A | ����������ͬ��Na2S2O3��Һ��H2SO4��Һ��Ӧ��������Һ���¶ȣ��������������ʱ������ | ��������������ʱ�����߷�Ӧ�¶ȣ���ѧ��Ӧ���ʼӿ� |
B | ��2.0 mLŨ�Ⱦ�Ϊ0.1 mol��L��1��KCl��KI�����Һ�еμ�1~2��0.01 mol��L��1AgNO3��Һ���������ʻ�ɫ | Ksp��AgCl��AgI |
C | 2NO2(g) | ��ѹƽ������������ɫ����ķ����ƶ� |
D | ��MgCl2��Һ���ɺ����գ��õ�MgO���� | ���ɵĹ�����ˮ�����ɵ�HCl�ӷ���ˮ���һ���ٽ�����Mg(OH)2�����պ����MgO |
A. A B. B C. C D. D