题目内容
【题目】一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2) 制取MnSO4·H2O并回收单质硫的工艺流程如下:
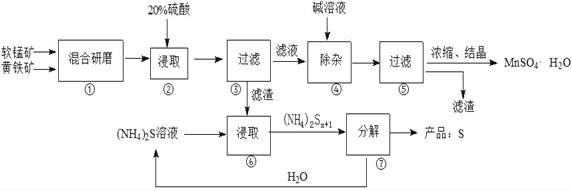
已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是_____________________________________________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为_____________________________________。
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入______________________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH为4~5,再继续煮沸一段时间,“继续煮沸”的目的是_____________________________________。步骤⑤所得滤渣为__________________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为_________________________________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=________________。
【答案】 增大接触面积,提高硫酸浸取时的浸取速率和浸取率 3MnO2+2FeS2+6H2SO4 =3MnSO4+Fe(SO4)3+4S↓+6H2O 软锰矿粉或H2O2溶液 破坏Fe(OH)3胶体并使沉淀颗粒长大,便于过滤分离 Fe(OH)3 (NH4)2Sx+1 ![]() 2NH3↑+H2S↑+xS↓ (8.25cV/a)%或(8.25cV×10-2)/a或0.0825cV/a或0.0825cV/a×100%
2NH3↑+H2S↑+xS↓ (8.25cV/a)%或(8.25cV×10-2)/a或0.0825cV/a或0.0825cV/a×100%
【解析】分析:两种矿物经粉碎研磨①与硫酸混合②,由于MnO2在酸性条件下具有氧化性,因此反应生成可溶性硫酸锰、硫酸铁和单质硫,③过滤后,滤液用碱液处理④除去铁元素⑤后,溶液经浓缩结晶得产品MnSO4·H2O,滤渣与(NH4)2S混合作用⑥后,经分解⑦处理得另一产品S,分解的其它产物可转化为(NH4)2S循环使用。
详解:(1) 步骤①混合研磨成细粉的主要目的是增大反应物的接触面积,提高硫酸浸取时的浸取速率和浸取率,提高原料的利用率;硫酸浸取时的反应方程式为3MnO2+2FeS2+ 6H2SO4 =3MnSO4+Fe2(SO4)3+4S↓+6H2O。
(2)由于Fe2+具有较强的还原性,在酸性条件下可用软锰矿粉(MnO2)或H2O2将其氧化为Fe3+,既不引入杂质,又能达到除去的目的;用碱液处理时,需将溶液加热至沸,然后在不断搅拌下调节pH为4~5,再继续煮沸一段时间,以破坏Fe(OH)3胶体并使沉淀颗粒增大,便于过滤分离,得到的滤渣为Fe(OH)3。
(3) 步骤⑦在90~100℃下进行,反应的化学方程式为(NH4)2Sx+1 ![]() 2NH3↑+H2S↑+xS↓。
2NH3↑+H2S↑+xS↓。
(4)已知本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。根据电子转移守恒可得二者反应的方程式为2KMnO4+3MnSO4·H2O=5MnO42+K2SO4+2H2SO4+H2O,已知n(KMnO4)=c mol/L×V×10-3L=cV×10-3mol,则n(MnSO4·H2O)=1.5cV×10-3mol,产品中Mn2+的质量分数为w(Mn2+)= [1.5cV×10-3mol×55g/mol]/ag×100%=(8.25cV/a)%。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案